无机物溶液的制造方法及无机物溶液的制造装置与流程-j9九游会真人
1.本发明涉及制造无机物溶液的制造方法及设备。
背景技术:
2.已知铍存在于be-si-o类矿石和be-si-al-o类矿石中。作为be-si-o类矿石的实例,可举出硅铍石(bertrandite)和似晶石(phenasite),作为be-si-al-o类矿石的实例,可举出绿柱石(beryl)和金绿玉(chrysoberyl)。以下将这些含有铍的矿石称为铍矿。此外,铍矿是铍的氧化物的一个例子。
3.当要制造铍、含铍化合物及含铍合金的任一者时,首先要将铍矿溶解在溶剂中来从铍矿中取出铍。然而,使铍矿溶解到溶剂中并不容易。作为易于溶解铍矿的溶剂,已知有硫酸等酸性溶液,但铍矿即使对酸性溶液也难溶。
4.因此,非专利文献1披露了一种能通过对铍矿进行烧结处理或熔融处理等预处理来使铍矿溶解到溶剂中的技术。
5.(现有技术文献)
6.非专利文献1:beryllium,[online],维基百科,[2019年6月25日检索],互联网《url:https://en.wikipedia.org/wiki/beryllium》
技术实现要素:
[0007]
(发明所要解决的问题)
[0008]
然而,将铍矿溶解于溶剂中的预处理需要很大的能量。根据非专利文献1的“制造”栏目,若进行烧结处理,则其温度例如为770℃,若进行熔融处理,则其温度例如为1650℃。
[0009]
本发明的一个方面的发明是鉴于上述问题而提出的,其目的是提供一种高能效的新型制造方法,其用以制造诸如铍矿这类既难溶于碱性溶液又难溶于酸性溶液的无机物的溶液。
[0010]
(用以解决问题的技术手段)
[0011]
为解决上述问题,本发明第1方面的无机物溶液制造方法包括:加热工序,对将无机物的粉末与氢氧化物混合而成的粉末状混合物进行介电加热,从而得到含有上述无机物的液状混合物。
[0012]
为解决上述问题,本发明第6方面的无机物溶液制造装置具备:混合部,其用以将无机物的粉末与氢氧化物混合来得到由无机物及氢氧化物组成的粉末状混合物;容器,其用以容纳所述粉末状混合物;电磁波产生部,其产生用于进行介电加热的电磁波。
[0013]
(发明效果)
[0014]
根据本发明的一个方面,能够制造诸如铍矿这类既难溶于碱性溶液又难溶于酸性溶液的无机物的溶液。
附图说明
[0015]
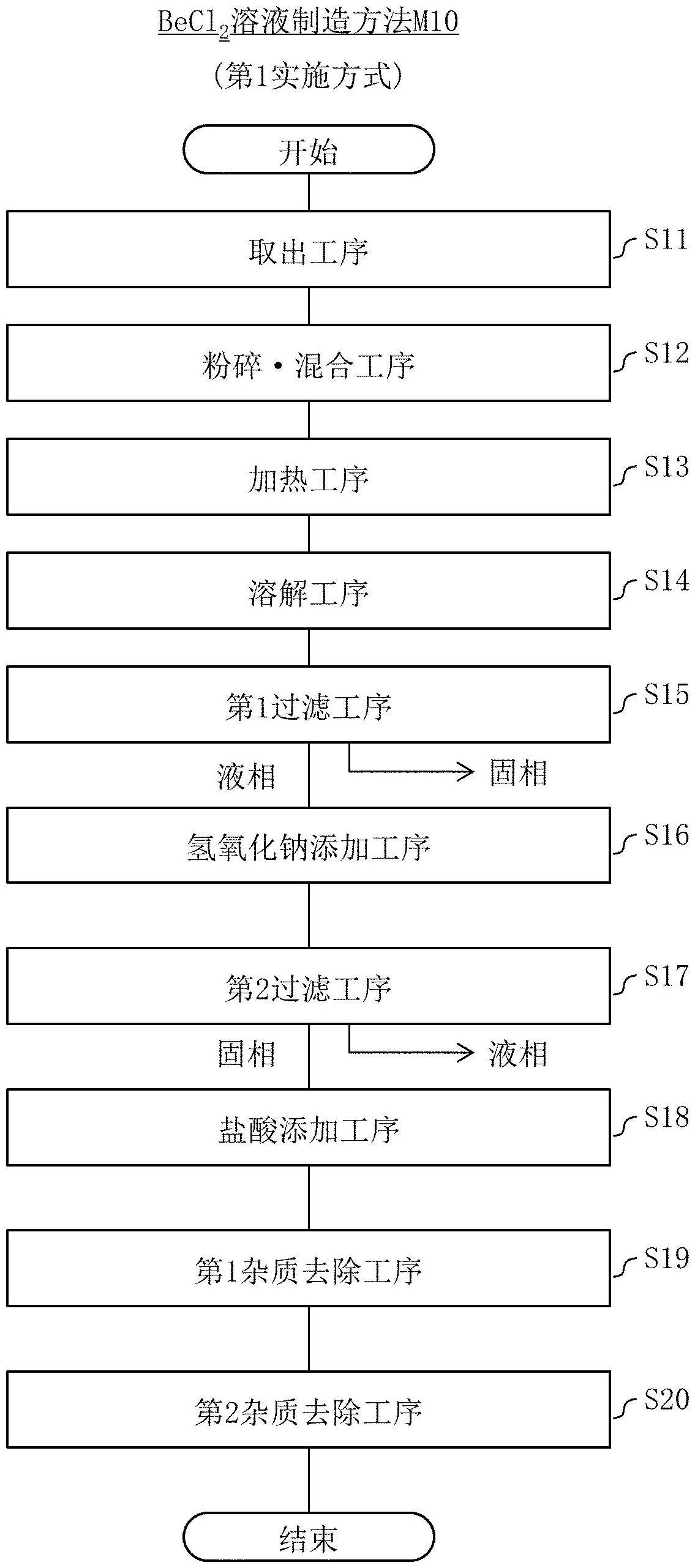
图1是本发明第1实施方式的铍溶液制造方法的流程图。
[0016]
图2是本发明第2~第4实施方式的铍制造方法、氢氧化铍制造方法以及氧化铍制造方法的流程图。
[0017]
图3是本发明第5实施方式中的钛及锂的分离方法的流程图。
[0018]
图4是本发明第6实施方式的介电加热装置的示意图。
[0019]
图5是具备图4所示介电加热装置的隔离器的斜视图。
[0020]
图6是在使用图4所示介电加热装置进行加热工序的情况下,铍矿与氢氧化钠所组成的混合物的温度与电磁波产生部的功率输出的关系图。
[0021]
图7是在使用图4所示介电加热装置对氢氧化钠单独进行介电加热的情况下,氢氧化钠的温度与电磁波产生部的功率输出的关系图。
[0022]
图8是在使用图4所示介电加热装置对碳酸钠单独进行介电加热的情况下,碳酸钠的温度与电磁波产生部的功率输出的关系图。
[0023]
图9是本发明第7实施方式的铍制造系统所具备的铍溶液制造装置的示意图。
[0024]
图10中,(a)是本发明第7实施方式的铍制造系统所具备的结晶装置、去水化装置以及电解装置的示意图,(b)是(a)所示结晶装置所具备的结晶处理槽的变形例的示意图,(c)是(a)所示去水化装置所具备的干燥机的变形例的示意图。
[0025]
图11中,(a)是本发明第8实施方式的氢氧化锂制造方法的流程图,(b)是本发明第9实施方式的碳酸锂制造方法的流程图。
[0026]
图12是本发明第10实施方式的碳酸锂制造方法的流程图。
[0027]
图13是本发明第11实施方式的碳酸锂制造方法的流程图。
[0028]
图14是本发明第12实施方式的氢氧化锂制造方法的流程图。
[0029]
图15是本发明第13实施方式的碳酸锂制造方法的流程图。
[0030]
图16是本发明第14实施方式的氢氧化锂制造方法的流程图。
[0031]
图17是本发明第15实施方式的镍化合物制造方法的流程图。
[0032]
图18是本发明第16实施方式中的铁分离方法的流程图。
[0033]
图19是第9实施例得到的独居石中的钇、镧、铈、钕、钐、铽、镝的溶解度的柱图。
[0034]
《附图标记说明》
[0035]
m10制造方法(无机物溶液的制造方法)
[0036]
s13 加热工序
[0037]
s14 溶解工序
[0038]
10,22介电加热装置(无机物溶液的制造装置)
[0039]
11,22a电磁波产生部
[0040]
12,22b波导管
[0041]
14,22c容器
[0042]
18隔离器
具体实施方式
[0043]
[第1实施方式]
[0044]
(铍溶液制造方法)
[0045]
结合图1,对本发明第1实施方式的铍溶液制造方法m10进行说明。图1是铍溶液制造方法m10的流程图。予以说明,铍溶液制造方法m10在后文中也简称为制造方法m10。本实施方式中,对铍盐酸盐即氯化铍(becl2)的水溶液、亦即becl2溶液的制造方法进行说明。becl2溶液是无机物溶液的一个例子。但使用制造方法m10制造的铍溶液不限于becl2溶液。例如,也可以是铍的硫酸盐即硫酸铍(beso4)的水溶液,亦即beso4溶液。还可以是铍的硝酸盐即硝酸铍(be(no3)2)的水溶液,亦即be(no3)2溶液。还可以是铍的氢氟酸盐即氟化铍(bef2)的水溶液,亦即bef2水溶液。还可以是铍的氢溴酸盐即溴化铍(bebr2)的水溶液,亦即bebr2水溶液。还可以是铍的氢碘酸盐即碘化铍(bei2)的水溶液,亦即bei2水溶液。
[0046]
本实施例中,采用废旧氚增殖材料和中子倍增材料作为制造方法m10所用的起始物料。但制造方法m10所用的起始物料不限是废旧氚增殖材料和中子倍增材料,可适当地从无机物中选用。在后文中,无机物是无机化合物和金属的总称。另外,无机化合物是指除有机物或有机化合物以外的化合物,即不含碳的化合物。无机化合物优选含有以后述稀有金属和稀土等为代表的金属。另外,所谓的金属包括贵金属。贵金属包括金(au)、银(ag)、白色金属(钌(ru)、铑(rh)、钯(pd)、锇(os),铱(ir)和铂(pt))。人们期望能从废旧催化剂(例如汽车尾气催化剂)和废电池(例如燃料电池)等中回收贵金属。氚增殖材料和中子倍增材料是无机物的一个例子。更具体地,氚增殖材料是复合氧化物的一个例子,中子倍增材料是金属间化合物的一个例子。这里,用作起始物料的无机物可以是诸如氚增殖材料和中子倍增材料的工业制造物,也可以是诸如后文所述矿石这类自然生成物。
[0047]
若例如将诸如铍矿这类既难溶于碱性溶液又难溶于酸性溶液的无机物作为起始物料,则制造方法m10很适用。铍矿是含有铍的矿石,已知有be-si-o类矿石和be-si-al-o类矿石。铍矿是硅酸盐矿物的一个例子。be-si-o类矿石例如有硅铍石(bertrandite)和似晶石(phenasite),be-si-al-o类矿石的实例包括绿柱石(beryl)和金绿玉(chrysoberyl)。铍矿是铍的氧化物的一个例子。当采用铍矿作为起始物料时,通过实施制造方法m10,可以获得例如becl2溶液。
[0048]
另外,在制造方法m10中,作为起始物料,可以采用含有一种或多种金属的矿石。此类矿石的一个例子有锂矿、白云石、铝土矿、磁铁矿、铬铁矿、铁矿石、钴矿、硫化物矿石、羟锰矿、辉钼矿、闪锌矿、重晶石、钽矿、铁锰矿、pgm矿、金红石、硅石、独居石、磷辉石、以及磷钇矿等。锂矿是含有锂(li)的硅酸盐矿物的一个例子。关于锂矿,已知有锂辉石(spodumene;lialsi2o6)。白云石是含有镁(mg)的碳酸盐矿物的一个例子。铝土矿含有铝(al)和镓(ga)。磁铁矿含有钒(v)。铬铁矿含有铬(cr)。铁矿石含有铁(fe)。钴矿含有钴(co)。硫化物矿石含有镍(ni)和锑(sb)。羟锰矿含有铌(nb)。辉钼矿含有钼(mo)。闪锌矿含有铟(in)。重晶石含有钡(ba)。钽矿含有钽(ta)。铁锰矿石含有钨(w)。pgm(pt族金属)矿石含有铂(pt)和钯(pd)。金红石是二氧化钛(tio2)晶体的一种形态,是具有四方晶系晶体结构的矿物。硅石是将硅酸质的矿物及岩石看作资源时的矿石名。硅石的主要成分是二氧化硅(sio2)。独居石含有稀土元素。稀土元素是钪(sc)、钇(y)和镧系元素的总称。独居石中的稀土元素例如有钇(y)、镧(la)、铈(ce)、钕(nd)、钐(sm)、铕(eu)、铽(tb)和镝(dy)。磷辉石含有钙(ca)。磷钇矿含有钇(y)。独居石、磷辉石和磷钇矿都是磷酸盐矿物的一个例子。
[0049]
含有一种或多种金属的矿石又称为多金属结核,如海底热液矿床、富钴结壳、锰结
核等。海底热液矿床含有铜、铅、锌等基质金属,还含有金、银等贵金属和稀有金属。富钴结壳含有镍、钴和铂等稀有金属。锰结核含有铜等基质金属、以及镍和钴等稀有金属。
[0050]
另外,在制造方法m10中,作为起始物料,也可以使用含有一种或多种金属的泥。作为含有一种或多种金属的泥,已知含有稀土(稀土类)元素的稀土泥。
[0051]
此外,在制造方法m10中,也可将玻璃用作起始物料。玻璃是与硅石同样地以二氧化硅(sio2)为主成分的氧化物的一个例子。这类玻璃有时还含有作为添加物的稀土元素。此外,关于氧化物的其它例子,例如有氧化铝(al2o3)和氧化镁(mgo)。氧化物还包括复合氧化物。复合氧化物是指,天然矿石以外的含有除氧以外的多种元素的氧化物。复合氧化物的例子有氧化钇稳定化型氧化锆(ysz)、堇青石(2mgo-2al2o
3-5sio2)。此外,在制造方法m10中,也可将陶瓷用作起始物料。陶瓷例如有氧化铝(al2o3)和氧化钛(tio2)。另外,以氧化钇稳定化型氧化锆、堇青石等为代表的复合氧化物也是陶瓷的一个例子。
[0052]
当采用这些矿石或泥作为起始物料时,通过实施制造方法m10,可以得到上述稀有金属和各稀土元素的例如盐酸盐溶液。
[0053]
此外,在制造方法m10中,也可将金属用作起始物料。关于金属的例子,可举出上述稀有金属和稀土。起始物料还可以是含有这些稀有金属和稀土中多种金属的合金。此外,关于稀土以外的金属的例子,可举出过渡金属。过渡金属例如有钛(ti)、铬(cr)、铁(fe)、钴(co)、镍(ni)、铜(cu)和锌(zn)。起始材料还可以是含有这些过渡金属中多种金属的合金。这种过渡金属制起始物料在机械和电子部件等的制造工序及加工工序等中多是以废渣的形式产生。这类废渣还包括称为淤积物的污泥或污水。此外,在冶炼金属时,淤积物以矿渣的形式产生。淤积物中含有的金属多种多样,其中一例是镍。当采用这些金属作为起始物料时,通过实施制造方法m10,可以获得上述稀有金属、稀土元素和过渡金属元素的例如盐酸盐溶液。因此能够回收这些金属。此外,当使用镍淤积物作为起始物料时,通过实施制造方法m10,能使镍淤积物中含有的非镍元素(如氟(f)和硫(s)等)溶解到盐酸盐溶液中。因此,可以提高镍淤积物中镍的纯度。
[0054]
如上所述,制造方法m10中的起始物料是多种多样的。若以施特伦茨分类来描述,则起始物料可以是氧化物、金属间化合物、硅酸盐矿物、复合氧化物、磷酸盐矿物、氧化物矿、多氧化物矿、硫化物矿、钨酸盐矿物和硫酸盐矿物中的任何一种。
[0055]
如图1所示,制造方法m10包括取出工序s11、粉碎
·
混合工序s12、加热工序s13、溶解工序s14、第1过滤工序s15、氢氧化钠添加工序s16、第2过滤工序s17、盐酸添加工序s18、第1杂质去除工序s19、第2杂质去除工序s20。
[0056]
(取出工序)
[0057]
取出工序s11是从核聚变反应堆的再生区中取出填充在该再生区中的氚增殖材料和中子倍增材料的工序。换句话说,是从再生区中取出废旧氚增殖材料和中子倍增材料的工序。在制造方法m10中,废旧氚增殖材料和中子倍增材料作为起始物料。
[0058]
氚增殖材料例如有锂氧化物。尤其可举出钛酸锂(li2tio3)、氧化锂(li2o)、铝酸锂(lialo2)以及硅酸锂(li2sio3和/或li4sio4)。此外,中子倍增材料例如有铍(be)、以及含铍的金属间化合物(be
12
ti和/或be
12
v,也称为beryllide)。氚增殖材料和中子倍增材料都形成为直径1mm左右的微小球状。在此基础上,再生区的内部还填充有尽可能均匀混合了的氚增殖材料和中子倍增材料。因此,在取出工序s11中从再生区取出的起始物料是由氚增殖材
料与中子倍增材料组成的混合物。本实施方式中,将钛酸锂用作一例氚增殖材料,将表面上形成有氧化层的铍用作一例中子倍增材料,以此来说明制造方法m10。予以说明,制造方法m10中用作起始物料的氚增殖材料和中子倍增材料各自并不限是钛酸锂和铍,能从上述的示例中适当选用。
[0059]
中子倍增材料即使是废旧铍,其大部分(例如98%左右)仍然是铍。因此,为了抑制核聚变反应堆的运用成本,迫切需要确立一种将高价的铍元素制成铍溶液后再重新利用的技术。此外,废旧铍的表面上形成有氧化铍(beo)层。因此,仅是将用过的铍浸渍在酸性溶液中,其所含的铍也几乎不溶解。
[0060]
如上所述,制造方法m10中所用的起始材料包括发挥中子倍增材料功能的以下至少一种:(1)铍;(2)含铍的金属间化合物;(3)表面上形成有氧化层的铍;(4)表面上形成有氧化层且含铍的金属间化合物。此外,制造方法m10中所用的起始材料也可进而包括发挥氚增殖材料功效的锂氧化物。
[0061]
此外,制造方法m10中所用的起始物料不限是核聚变反应堆中废旧中子倍增材料和氚增殖材料。该起始材料也可以是核聚变领域以外的核能领域和加速器领域中的废旧铍及其合金。还可以是一般工业领域中产生的作为工业废料的铍及其合金。根据制造方法m10,可以将(1)核聚变反应堆中产生的废旧中子倍增材料和氚增殖材料、(2)核聚变领域以外的核能领域和加速器领域中产生的废旧中子反射件、废旧中子减速材料、以及曾作为中子源的废旧靶材料等中所含的铍及其合金、(3)一般工业领域中产生的作为工业废料的铍及其合金,不加区分地进行处理来制造新的铍。此外,根据制造方法m10,能去除这些起始物料中所含的作为杂质的铀和其他元素等。
[0062]
(粉碎
·
混合工序)
[0063]
粉碎
·
混合工序s12是在取出工序s11之后实施的工序。在粉碎
·
混合工序s12中,首先通过粉碎起始物料来获得起始物料的粉末。即,通过粉碎起始物料来减小起始物料的粒径,且在即使中子倍增材料表面上形成有氧化层的情况下,也通过机械性破坏该氧化层来使被氧化层覆盖的铍露出。用于粉碎起始物料的技术并无限定,可以从已知技术中适当选择,例如有球磨法。
[0064]
此外,在粉碎
·
混合工序s12中,通过粉碎氢氧化钠(naoh)来获得氢氧化钠粉末。但如果购买粉末状氢氧化钠来使用,则可以省略粉碎
·
混合工序s12中的粉碎氢氧化钠的步骤。此外,若粉碎
·
混合工序s12中所用的氢氧化钠为颗粒状或片状,则可以省略粉碎
·
混合工序s12中的粉碎氢氧化钠的处理。粉碎
·
混合工序s12中所用的氢氧化钠的形状不受限制。予以说明,氢氧化钠是氢氧化物的一个例子。制造方法m10中所用的氢氧化物不限是氢氧化钠,可以是氢氧化锂(lioh)、氢氧化钾(koh)、氢氧化钙(ca(oh)2)和氢氧化锶(sr(oh)2)中的至少一种。
[0065]
粉碎
·
混合工序s12中,在上述基础上,通过将起始物料的粉末与氢氧化钠(本实施例中为氢氧化钠的粉末)混合,获得起始物料和氢氧化钠的粉末状混合物。以下,起始物料和氢氧化钠的粉末状混合物也简单地描述为粉末状混合物。
[0066]
(加热工序s13)
[0067]
加热工序s13是在粉碎
·
混合工序s12之后对粉末状混合物进行介电加热来将起始物料和氢氧化钠熔融的工序。通过实施加热工序s13,氢氧化钠将后述的电磁波能量转换
为热量,其结果,得到含有起始物料和氢氧化钠的液状混合物。以下,起始物料和氢氧化钠的液状混合物也简单地描述为液状混合物。由于起始物料和氢氧化钠不含水分,因此即使粉末状混合物或液状混交物的温度超过100℃,也无需担心水分沸腾。因此,加热工序s13中能在常压下对粉末状混合物进行介电加热。通过加热工序s13获得的液状混合物为乳液状态,随着温度的降低,至少其一部分有时会从乳液状态变为固体状态。
[0068]
介电加热是通过向对象物施加具有规定频率的电磁波来加热对象物的技术的总称。其中,视施加的电磁波的频带,有时称为高频加热,有时称为微波加热。例如,高频加热是将3mhz以上且300mhz以下的频带内的电磁波(所谓的短波或超短波)施加给对象物,而微波加热是将300mhz以上且低于30ghz的频带内的电磁波(所谓的微波)施加给对象物。家庭中也普及的微波炉就是能够实施微波加热的装置的一个例子。
[0069]
本实施方式中,在加热工序s13中向粉末状混合物施加频率为2.45ghz的电磁波。稍后将结合图5或图9来说明用于向粉末状混合物施加电磁波的装置的结构。
[0070]
利用介电加热法来对粉末状混合物进行加热,则能以比以往更高的能效将起始物料和氢氧化钠转变为可溶于酸性溶液的液状混合物。如后文所述,由于液状混合物易溶解于酸(在本实施例中为盐酸)溶液,因此能得到溶解有氯化铍水合物(becl
2-xh2o)及氯化锂(licl)的盐酸溶液。因此,制造方法m10可提供一种高能效的新型制造方法。
[0071]
予以说明,加热工序s13中的加热温度可以适当设定。但加热工序s13中的加热温度优选为用以容纳粉末状混合物的容器(例如第7实施方式中记载的容器14)的耐热温度以下。例如,该容器若是如容器14那样由聚四氟乙烯制成,则加热工序s13中的加热温度优选为250℃以下。加热温度的一个例子是220℃。构成容器的材料若具有抗酸性溶液的耐腐蚀性且耐热温度高于250℃,则加热工序s13中的加热温度也可以高于250℃。关于耐热温度高于250℃的材料,例如可举出氧化铝(al2o3)和氮化硼(bn)等。若采用由氧化铝或氮化硼等构成的容器,则加热工序s13中的加热温度也可以高于250℃。关于使用这种容器时的加热温度,例如可举出300℃。通过提高加热工序s13中的加热温度,很有可能缩短加热工序s13所需的时间。此外,可以适当地设定加热工序s13中的加热时间。加热时间的一个例子是8分钟。
[0072]
在加热工序s13的一个变型中,也可以在对粉末状混合物进行介电加热前向粉末状混合物添加少量水。在介电加热中,水可以有效地吸收施加到粉末状混合物的微波并将其转化为热量。因此,通过向粉末状混合物中添加少量水,粉末状混合物的温度可以很快被加热到所需的温度(例如250℃)。虽然添加给粉末状混合物的水量不受限制,但优选相对于粉末状混合物的质量为5wt%以上。
[0073]
(溶解工序)
[0074]
溶解工序s14是在加热工序s13之后实施的工序。溶解工序s14是通过将在加热工序s13中获得的液状混合物溶解在酸(本实施例中为盐酸(hcl))溶液中,从而获得起始物料中所含金属的盐酸溶液的工序。在本实施例中,获得溶解有氯化铍水合物(becl2·
xh2o)和氯化锂(licl)的盐酸溶液。溶解工序s14中使用的酸溶液不限于盐酸溶液,也可以是硫酸(h2so4)溶液、硝酸溶液、氢氟酸溶液、氢溴酸溶液、以及氢碘酸溶液中的至少任一种。还可以是混合这些酸溶液当中的多种酸溶液而获得的混合酸溶液。作为这种混合酸溶液,例如可举出混合浓盐酸和浓硝酸而得到的王水。此外,在溶解工序s14中,水可以用作溶解在加热
工序s13中获得的液状混合物的液体。
[0075]
在溶解工序s14中,液状混合物可溶解于常温且常压下的盐酸溶液。但还能通过提高盐酸溶液的温度来促进液状混合物相对于盐酸溶液的溶解。作为加热盐酸溶液的装置,加热工序s13所用的施加电磁波的装置为良选。这里,在溶解工序s14中,为了抑制盐酸溶液的沸腾,优选将盐酸溶液的温度设定为小于100度。由此,不需要对盐酸溶液进行加压,从而在常压下就能实施溶解工序s14。
[0076]
(第1过滤工序)
[0077]
第1过滤工序s15是在溶解工序s14之后实施的工序。第1过滤工序s15是使用过滤器将含锂的铍溶液中所含的固相与液相彼此分离的工序。固相中含有一部分钛酸锂和氧化钛。在作为酸性溶液的液相中,主要含有氯化铍水合物及氯化锂。
[0078]
通过实施第1过滤工序s15,能够容易地将液相中所含的氯化铍水合物及氯化锂与固相中所含的氧化钛彼此分离。
[0079]
(氢氧化钠添加工序)
[0080]
氢氧化钠添加工序s16是在第1过滤工序s15之后实施的工序。氢氧化钠添加工序s16是:将经第1过滤工序s15而分离得到的酸性溶液的极性从酸性途经中性化而调整为碱性的工序。换言之,氢氧化钠添加工序s16是:将含有液相氯化铍水合物及液相氯化锂且不含固相氧化钛的酸性溶液的极性,从酸性途经中性化而调节为碱性的工序。
[0081]
在本实施方式中,氢氧化钠添加工序s16规定为:对经第1过滤工序s15而分离得到的酸性溶液添加氢氧化钠水溶液。其结果,经第1过滤工序s15而分离得到的溶液的极性从酸性途经中性(ph7)而变为碱性,于是该溶液中含有的氯化铍水合物变成氢氧化铍(be(oh)2),并作为固相而沉淀在碱性溶液中。这里,氯化锂因溶解在碱性溶液中而不出现沉淀。也就是说,即使在实施了氢氧化钠添加工序s16后,氯化锂也以氢氧化锂的方式而仍留在液相中。
[0082]
(第2过滤工序)
[0083]
第2过滤工序s17是在氢氧化钠添加工序s16之后实施的工序。第2过滤工序s17是使用过滤器将氢氧化钠添加工序s16中得到的碱性溶液所含的固相和液相分离的工序。该固相中含有氢氧化铍,该液相中含有氢氧化锂。
[0084]
通过实施第2过滤工序s17,能够容易地分离固相中所含的氢氧化铍和液相中所含的氢氧化锂。
[0085]
(盐酸添加工序)
[0086]
盐酸添加工序s18是在第2过滤工序s17之后实施的工序。盐酸添加工序s18是:在经第2过滤工序s17而得的氢氧化铍中添加hcl溶液,从而使铍以氯化铍水合物的形态来再次溶解进酸性溶液中的工序。hcl溶液中hcl的浓度可适当调整,但最好调整成ph值为1以下。
[0087]
通过实施盐酸添加工序s18,可以得到溶解有氯化铍水合物的盐酸溶液(也称为铍溶液或becl2溶液)。
[0088]
(第1杂质去除工序)
[0089]
第1杂质去除工序s19是在盐酸添加工序s18之后实施的工序。第1杂质去除工序s19是使用可吸附第1元素的有机化合物来从经盐酸添加工序s18而得的铍溶液中将上述第
1元素去除的工序。
[0090]
第1杂质去除工序s19中所被去除的第1元素随在此所用的有机化合物而定。作为在第1杂质去除工序s19中可利用的有机化合物,可以举出氧化三正辛基膦(topo,tri-n-octylphosphine oxide)、二(2-乙基己基)磷酸(d2ehpa,di-(2-ethylhexyl)phosphoric acid)、磷酸三丁酯(tbp,tri-n-butyl phosphate)、以及乙二胺四乙酸(edta,ethylenediaminetetraacetic acid)。另外,作为在第1杂质去除工序s19中可利用的市售有机化合物,可以举出eichrom technologies公司的uteva(注册商标)树脂。
[0091]
topo能吸附al、au、co、cr、fe、hf、re、ti、uo
22
、v、zr、稀土元素和锕系元素。d2ehpa能吸附u、co、ni、mn等。tbp能吸附u、th等。edta系能吸附mg、ca、ba、cu、zn、al、mn、fe等。uteva(注册商标)树脂能吸附u、th、pu、am等。这些元素是第1元素的示例。
[0092]
这些有机化合物溶解于有机溶剂(例如煤油、环己烷、苯等)。通过将溶解有这些有机化合物的溶液(以下也称有机化合物溶液)混合到实施了盐酸添加工序s18后而得的hcl溶液中,并进行搅拌,来使有机化合物对第1元素进行吸附。
[0093]
在第1杂质去除工序s19中,与有机化合物溶液混合的hcl溶液的液性优选为酸性,更优选其ph值为2以下。通过该方案,有机化合物不会吸附铍,从而能够提高有机化合物吸附第1元素的效率。予以说明,hcl溶液的液性越接近中性,有机化合物吸附铍的效率越高,并且吸附第1元素的效率越低。
[0094]
本实施方式中,作为在第1杂质去除工序s19中使用的有机化合物和有机溶剂,采用的是topo和煤油。但有机化合物和有机溶剂各自并不限是topo和煤油,可以从前文的示例当中适当地组合选用。
[0095]
经盐酸添加工序s18而得的作为水溶液的铍溶液、以及有机化合物溶液通过放置一段时间而分离为两层。因此,可以容易地将实施第1杂质去除工序s19而得的第1元素含量得以抑制了的铍溶液,与含有第1元素的有机化合物溶液彼此分离。
[0096]
通过实施第1杂质去除工序s19,可以降低铍溶液中所含的第1元素的浓度。其结果,在将起始物料溶解于酸性溶液来制造铍溶液的情况下,即使起始物料中含有如上所述的除铍以外的元素即第1元素,也能够降低由铍溶液来制造铍、氢氧化铍以及氧化铍的任一种的情况中的第1元素的浓度。关于第1元素的例子,可以举出铀、钍、钚、镅等。
[0097]
作为具体例,在采用由包括第1杂质去除工序s19的制造方法m10所制得的氯化铍来制造铍的情况下,能将铍中所含的铀的浓度抑制为低于0.7ppm。铀浓度低于0.7ppm的铍即使在核聚变反应堆中作为中子倍增材料来使用,其使用后的铀浓度也低于用以判定是否适合陆地浅埋处理的阈值。因此,本发明一个方面所包含的铍即使在核聚变反应堆中用作中子倍增材料,也可以直接进行陆地浅埋处理。
[0098]
(第2杂质去除工序)
[0099]
第2杂质去除工序s20是在第1杂质去除工序s19之后实施的工序。第2杂质去除工序s20是:将经盐酸添加工序s18而得的铍溶液的极性从酸性途经中性化来调整为碱性,从而从铍溶液中去除第2元素的工序。本实施方式的说明中,是在盐酸添加工序s18之后依次进行第1杂质去除工序s19和第2杂质去除工序s20的,但第1杂质去除工序s19和第2杂质去除工序s20的顺序也可以互换。
[0100]
本实施方式中,在第2杂质去除工序s20中,向实施了盐酸添加工序s18后的铍溶液
中添加碳酸氢钠(nahco3)直至饱和。其结果,途经中性(ph7)化后,该铍溶液中的除铍以外的元素(例如al、fe等)变成氢氧化物(例如al(oh)3、fe(oh)3等)并沉淀在该铍溶液中。这里,即使在碳酸氢钠饱和的状态下,be(oh)2也溶解在铍溶液中而不发生沉淀。铝(al)和铁(fe)是第2元素的示例。
[0101]
通过实施第2杂质去除工序s20而沉淀在铍溶液中的除铍以外的元素的氢氧化物能通过对铍溶液进行过滤来容易地从铍溶液中去除。
[0102]
另外,在通过实施第2杂质去除工序s20而去除了第2元素后的铍溶液中,优选另行添加hcl。因此,通过将hcl另行添加到铍溶液中,be(oh)2溶液的极性便途经中性化而调整为酸性,并且溶液中生成高纯度的氯化铍水合物(becl2·
xh2o)。
[0103]
通过如此地进行第2杂质去除工序s20,能降低铍溶液中所含的第2元素的浓度。其结果,在通过将起始物料溶解于酸性溶液中来制造铍溶液的情况下,即使起始物料中含有如上所述的除铍以外的元素即第2元素,也能够降低用铍溶液来制造铍、氢氧化铍及氧化铍的任一种的情况中的第2元素的浓度。
[0104]
如上所述,在制造方法m10中,加热工序s13中优选通过施加微波来对含有氧化铍的酸性溶液进行介电加热。
[0105]
此外,当制造方法m10包括预加热工序时,与加热工序s13类似地,预加热工序中优选通过施加微波来对含有氧化铍的碱性溶液进行介电加热。
[0106]
利用微波的介电加热(即微波介电加热)技术是微波炉中应用的技术,即是广泛普及的技术。因此,与以往的制造方法相比,制造方法m10可以削减实施所需成本。
[0107]
如上所述,在制造方法m10中,所述铍溶液优选为氯化铍溶液。
[0108]
根据制造方法m10,可以在不经由氢氧化铍的情况下容易地制造氯化铍溶液。如下所述,可以很容易地由氯化铍溶液来制造铍、氢氧化铍及氧化铍。因此,氯化铍溶液适合作为铍溶液。
[0109]
(铍溶液制造方法的变形例)
[0110]
如上所述,在本实施例中描述了使用废旧的氚增殖材料和中子倍增材料作为起始物料的制造方法m10。而在本变形例中,将简要描述使用绿柱石作为起始物料时的制造方法m10。绿柱石是be-si-al-o类铍矿的一种形态,是无机物的一个例子。也就是说,绿柱石不仅含铍,还含硅(si)和铝(al)。起始材料也可以含有除绿柱石以外的矿石(例如后述的锂辉石)。
[0111]
在本变形例中,由于使用从矿山开采的绿柱石作为起始物料,因此可以省略取出工序s11。
[0112]
在粉碎
·
混合工序s12中,通过粉碎绿柱石来获得绿柱石粉末。类似地,通过粉碎氢氧化钠来获得氢氧化钠粉末。在此基础上,通过混合绿柱石粉末和氢氧化钠粉末来获得绿柱石与氢氧化钠的粉末状混合物。予以说明,在本变形例中,氢氧化钠的形状不限是粉末。
[0113]
关于加热工序s13和溶解工序s14,与前文结合图1所说明过的内容相同。在加热工序s13中,进行介电加热来使混合物的温度为220度,并且加热时间为8分钟。通过加热工序s13所获得的液状混合物是白浊的乳液状。
[0114]
另外,由于绿柱石的熔点为1410℃,氢氧化钠的熔点为318℃,因此与这些熔点相
比,加热工序s13中的加热温度较低。但绿柱石和氢氧化钠即使在这种加热情况下仍可熔融,认为其理由在于伴随电磁波的施加,熔解得到了促进。在制造方法m10中,由于将粉状的绿柱石与氢氧化钠混合,因此施加的电磁波直接作用于粉状混合物的内部,从而可以直接加热内部。另外,根据预计,在粉状混合物内部会伴随电磁波的施压而产生放电,认为该放电也促进了熔解。其结果,在制造方法m10中,尽管是220℃的低温度,也能使绿柱石变化成能溶解于盐酸溶液的状态。在非专利文献1记载的技术中,在例如2000℃左右的高温下来使绿柱石熔融。而与该技术相比,制造方法m10能够将消耗能量抑制在约1/10000(0.01%)。
[0115]
予以说明,即使实施了加热工序s13和溶解工序s14后,绿柱石含有的硅也以固体氧化物的状态残留在盐酸溶液中。因此,能通过实施第1过滤工序s15来从氯化铍溶液中去除硅。
[0116]
在使用绿柱石作为起始物料的情况下,可以省略氢氧化钠添加工序s16、第2过滤工序s17以及盐酸添加工序s18。
[0117]
在使用铍作为起始物料的情况下,同样优选实施第1杂质去除工序s19和第2杂质去除工序s20。通过进行第1杂质去除工序s19,能够降低氯化铍液中所含的第1元素(例如铀、钍、钚、镅等)的浓度。另外,通过实施第2杂质去除工序s20,能够降低氯化铍溶液中所含的第2元素(例如铝、铁等)的浓度。绿柱石中虽含有铝,但通过实施第2杂质去除工序s20,能够切实地从氯化铍溶液中去除铝。
[0118]
通过如上述那样实施本变形例,能将绿柱石用作起始物料,并在不经由氢氧化铍的情况下容易地制造无机物溶液的一例、即氯化铍溶液。
[0119]
(锂溶液制造方法)
[0120]
在上述的铍溶液制造方法的变形例中,使用绿柱石作为起始物料,得到溶解有氯化铍水合物(becl2·
xh2o)的盐酸溶液。而接下来,将简要说明使用锂矿石作为起始物料,来获得溶解有锂盐酸盐即氯化锂(licl)的盐酸溶液的情况。本制造方法在上述铍溶液制造方法的变形例的基础上将起始物料从绿柱石改为了锂矿石。因此该制造方法也可以称为铍溶液制造方法的一个变型例。
[0121]
在本制造方法中,对作为锂盐酸盐的氯化锂(licl)的水溶液、即licl溶液的制造方法进行说明。licl溶液是无机物溶液的一个例子。但使用本制造方法制造的锂溶液并不限是licl溶液。例如,也可以是作为锂硫酸盐的硫酸锂(li2so4)的水溶液、即li2so4溶液。也可以是作为锂硝酸盐的硝酸锂(lino3)的水溶液、即lino3溶液。也可以是锂的氢氟酸盐,即氟化锂(lif)。也可以是锂的氢溴酸盐,即溴化锂(libr)。可以是锂的氢碘酸盐,即碘化锂(lii)。
[0122]
锂矿石是含锂的矿石的总称,也是锂氧化物的一个例子。锂矿石具有结晶性。锂矿石包括锂辉石(spodumene;lialsi2o6)、锂云母(lepidolite,k(al,li)2(si,al)4o
10
(oh,f)2)、透锂长石(petalite,lialsi4o
10
)和锂电石(elbaite,na(li,al)3al6(bo3)3si6o
18
(oh)4)。在本制造方法中,作为起始物料的一个例子,采用锂矿石的一种形态即锂辉石。现有技术中,为了使锂辉石溶解于溶液,是在1000℃以上的温度下进行煅烧处理的。
[0123]
粉碎
·
混合工序s12中,通过粉碎锂辉石来获得锂辉石粉末。类似地,通过粉碎氢氧化钠来获得氢氧化钠粉末。在此基础上,通过混合锂辉石粉末和氢氧化钠粉末来获得绿柱石与氢氧化钠的粉末状混合物。予以说明,在本变形例中,氢氧化钠的形状不限是粉末。
[0124]
关于加热工序s13和溶解工序s14,与前文结合图1所说明过的内容相同。
[0125]
予以说明,即使实施了加热工序s13和溶解工序s14后,锂辉石含有硅也以固体氧化物的状态残留在盐酸溶液中。因此,能通过实施第1过滤工序s15来从锂溶液中去除硅。
[0126]
在使用锂辉石作为起始物料的情况下,可以省略氢氧化钠添加工序s16、第2过滤工序s17以及盐酸添加工序s18。
[0127]
在使用锂辉石作为起始物料的情况下,同样优选实施第1杂质去除工序s19和第2杂质去除工序s20。通过进行第1杂质去除工序s19,能够降低锂溶液中所含的第1元素(例如铀、钍、钚、镅等)的浓度。另外,通过实施第2杂质去除工序s20,能够降低锂溶液中所含的第2元素(例如铝、铁等)的浓度。锂辉石中虽含有铝,但通过实施第2杂质去除工序s20,能够切实地从锂溶液中去除铝。
[0128]
(第2~第4实施方式)
[0129]
结合图2的(a)~(c),说明本发明第2~第4实施方式各自的铍(be)制造方法m20、氢氧化铍(be(oh)2)制造方法m30、以及氧化铍(beo)制造方法m40。图2中的(a)~(c)分别是铍制造方法m20、氢氧化铍制造方法m30及氧化铍制造方法m40各自的主要部分的流程图。以下,将铍制造方法m20、氢氧化铍制造方法m30和氧化铍制造方法m40分别简称为制造方法m20、制造方法m30和制造方法m40。
[0130]
(铍制造方法m20)
[0131]
如图2所示,制造方法m20包括:图1所示制造方法m10中的取出工序s11、粉碎
·
混合工序s12、加热工序s13、溶解工序s14、第1过滤工序s15、氢氧化钠添加工序s16、第2过滤工序s17、第1杂质去除工序s19、第2杂质去除工序s20;去水化工序s21;电解工序s22。以下,也将取出工序s11、加热工序s13、第1过滤工序s15、氢氧化钠添加工序s16、第2过滤工序s17、第1杂质去除工序s19及第2杂质去除工序s20简称为各工序s11~s20。
[0132]
制造方法m20所包括的、制造方法m10中各工序s11~s20与第1实施方式中说明过的各工序s11~s20同样。因此这里省略工序s11~s20的说明。即,设想已得到了becl2溶解于hcl溶液中而成的becl2溶液,并在此基础上仅对制造方法m20中的去水化工序s21和电解工序s22进行说明。
[0133]
去水化工序s21是:对经制造方法m10的各工序s11~s20而得的becl2溶液中所含的氯化铍水合物(becl2·
xh2o)实施去水化,从而生成作为一例铍盐的becl2的工序。
[0134]
在去水化工序s21中,将氯化铵加入氯化铍水合物中,并在真空中以90℃加热氯化铍水合物24小时,从而能使含水量无限接近0。也就是说,能够实现氯化铍水合物的去水化。
[0135]
氯化铵与氯化铍水合物中的水分发生反应而生成氢氧化铵和盐酸。而生成的氢氧化铵与盐酸会再次反应,从而一边释放水,一边变回氯化铵。通过这样的过程,可以由氯化铍水合物来获得完成了去水化的氯化铍。
[0136]
另外,去水化工序s21中的加热温度不限是90℃,可以从80℃以上且110℃以下的温度范围中适当地选择。但加热温度过高时,氯化铍水合物的去水化很可能不充分。因此,该加热温度优选为80℃以上且90℃以下,更优选是90℃。
[0137]
另外,在去水化工序s21中实施去水化处理的时间不限是24小时,可以适当地选定。
[0138]
电解工序s22是对经去水化工序s21而得的becl2进行熔盐电解来生成金属铍的工
序。
[0139]
通过如上述那样实施制造方法m20,能从起始物料来制造金属铍。
[0140]
(氢氧化铍制造方法m30)
[0141]
如图2所示,制造方法m30包括制造方法m10中各工序s11~s20、以及中和工序s31。与制造方法m20的情况同样,这里仅说明中和工序s31。
[0142]
中和工序s31是:用碱来对经制造方法m10的各工序s11~s20而得的becl2溶液中所含的becl2·
xh2o进行中和,从而生成be(oh)2的工序。
[0143]
通过如上述那样实施制造方法m30,能从起始物料来制造be(oh)2。
[0144]
(氧化铍制造方法m40)
[0145]
如图2所示,制造方法m40包括制造方法m10中各工序s11~s20、以及加热工序s41。与制造方法m20的情况同样,这里仅说明加热工序s41。
[0146]
加热工序s41是:对经制造方法m10的各工序s11~s20而得到becl2溶液进行加热,从而生成beo的第3加热工序。通过该工序,溶解在becl2溶液中的becl2·
xh2o被水解,从而生成beo。
[0147]
通过如上述那样实施制造方法m40,能从起始物料来制造beo。
[0148]
(小结)
[0149]
根据这些制造方法m20、m30、m40,能够采用高能效的新型制造方法来制造铍、氢氧化铍以及氧化铍的各者。去水化工序s21、电解工序s22、中和工序s31及加热工序s41各自均可利用已知技术来实施。
[0150]
[第5实施方式]
[0151]
(钛及锂的分离方法m50)
[0152]
结合图3,对本发明第5实施方式的钛及锂的分离方法m50进行说明。图3是钛及锂的分离方法m50的流程图。以下,将钛及锂的分离方法m50简称为分离方法m50。
[0153]
如图3所示,分离方法m50包括:图1所示制造方法m10中的取出工序s11、粉碎
·
混合工序s12、加热工序s13、溶解工序s14、第1过滤工序s15;粉碎工序s51;盐酸浸渍工序s52;第3过滤工序s53。以下,也将取出工序s11、粉碎
·
混合工序s12、加热工序s13、溶解工序s14及第1过滤工序s15简称为各工序s11~s15。
[0154]
分离方法m50所包括的、制造方法m10中各工序s11~s15与第1实施方式中说明过的各工序s11~s15同样。因此这里省略工序s11~s15说明。即,设想液相中所含的氯化铍水合物及氯化锂与固相中所含的钛酸锂已彼此分离,并在此基础上仅对分离方法m50中的粉碎工序s51、盐酸浸渍工序s52和第3过滤工序s53进行说明。予以说明,实施第1过滤工序s15后的固相中不仅可含有钛酸锂,还可含有氧化钛。
[0155]
粉碎工序s51是:对实施了第1过滤工序s15后的固相中所含的钛酸锂进行粉碎,从而减小钛酸锂的粒径的工序。用于粉碎钛酸锂的技术并无限定,可以从已知技术中适当选择,例如有球磨法。
[0156]
如果能将钛酸锂粉碎得更细,就能增大其表面积相对于钛酸锂总体积的比例,因此在后述的盐酸浸渍工序s52中,使钛酸锂所含的锂溶解到溶液中的所需时间有望缩短。另一方面,若将钛酸锂粉碎得过细,则粉碎工序s51的所需时间和成本会增加。因此,优选在考虑盐酸浸渍工序s52的所需时间、粉碎工序s51的所需时间、粉碎工序s51的所需成本等的基
础上,来决定粉碎工序s51实施后的钛酸锂的粒径。
[0157]
作为钛酸锂的粒径,可以采用平均粒径、众数粒径和中位粒径中的任一种。在测得了钛酸锂的粒径分布的情况下,平均粒径是与粒径分布之平均值相对应的粒径,众数粒径是粒径分布中出现频度最高的粒径,中位粒径是粒子直径分布中的与累积频度50%之处相对应的粒径。
[0158]
本实施例中,以钛酸锂的平均粒径达到100μm的方式来实施粉碎工序s51。
[0159]
盐酸浸渍工序s52是在粉碎工序s51之后实施的工序。盐酸浸渍工序s52是将经粉碎工序s51而粉碎后的钛酸锂浸渍在盐酸溶液中的工序。通过实施盐酸浸渍工序s52,钛酸锂所含的锂以氯化锂的形式溶解在盐酸溶液中,而钛酸锂所含的钛以氧化钛(例如tio2)的形式残留在盐酸溶液中。因此,在实施盐酸浸渍工序s52之后,盐酸溶液包含固相中所含的氧化钛和液相中所含的氯化锂。
[0160]
若想更快地使钛酸锂所含的锂溶解到盐酸溶液中,那么可以运用与加热工序s13相同的方法,来对含有钛酸锂的盐酸溶液进行介电加热。
[0161]
第3过滤工序s53是在盐酸浸渍工序s52之后实施的工序。第3过滤工序s53是使用过滤器来将固相中所含的氧化钛与液相中所含的氯化锂彼此分离的工序。
[0162]
通过实施第3过滤工序s53,能容易地将固相中所含的氧化钛与液相中所含的氯化锂彼此分离。
[0163]
经第3过滤工序s53而分离得到的含有氯化锂的酸性溶液优选与经第1过滤工序s15而分离得到的酸性溶液同样地,提供给氢氧化钠添加工序s16。通过将经第1过滤工序s15而分离得到的固相中所含的锂以氯化锂的形态分离出来,并将该氯化锂提供给氢氧化钠添加工序s16,能够更有效地回收锂化合物。换句话说,分离方法m50中的粉碎工序s51、盐酸浸渍工序s52以及第3过滤工序s53可以与制造方法m10的一部分进行组合。
[0164]
通过如上述那样实施分离方法m50,可以将钛酸锂所含的钛及锂各自以氧化钛及氯化锂的形态分离出来。因此,锂这一宝贵资源可以与钛一起回收和再利用。
[0165]
(第6实施形态)
[0166]
结合图4及图5,对本发明第6实施方式的介电加热装置10进行说明。介电加热装置10是本发明一个方面的铍溶液制造装置的示例。图4是介电加热装置10的示意图。介电加热装置10是用来实施图1所示制造方法m10中的加热工序s13、以及图3所示分离方法m50中的加热工序s13的加热装置。此外,若要在制造方法m10的溶解工序s14中加热盐酸溶液,则此加热也能够采用介电加热装置10。
[0167]
如在第1实施方式中说明的那样,介电加热根据所施加的电磁波的频带而分类为高频加热或微波加热的某一种。介电加热装置10是向对象物实施高频加热与微波加热当中的微波加热的装置。
[0168]
《介电加热装置的构成》
[0169]
如图4所示,介电加热装置10具备电磁波产生部11、波导管12、电磁波施加部13、容器14、旋转台15、搅拌子16和温度计17。此外,如图5所示,还具备隔离器18。另外,介电加热装置10还具备图4中未示出的控制部。
[0170]
(电磁波产生部)
[0171]
电磁波产生部11构成为产生具有规定频率的电磁波。规定频率例如可以在微波频
带内适当选择,但在本实施方式中,采用2.45ghz作为规定频率。2.45ghz的频率与家用微波炉中采用的电磁波频率相同。
[0172]
(波导管)
[0173]
波导管12是金属制圆柱形构件。波导管12的一端连接到电磁波产生部11,波导管12的另一端连接到用以容纳后述容器14的电磁波施加部13。也就是说,波导管12介于电磁波产生部11和容器14之间。波导管12将电磁波产生部11产生的电磁波,从波导管12的一端传导到波导管12的另一端。并且波导管12将该电磁波,从波导管12的另一端辐射到用以容纳容器14的电磁波施加部13的内部空间。也就是说,波导管12沿着从电磁波产生部11前往容器14的方向来传导电磁波产生部11产生的电磁波。
[0174]
(隔离器)
[0175]
如图5所示,在波导管12的中途区段设有隔离器18。隔离器18具备循环器181、虚设负载182、冷却管183。循环器181插入在波导管12的中途区段。
[0176]
循环器181具备磁铁(例如铁氧体制),如图5所示,具备3个端口p1~p3。电磁波产生部11隔着波导管12的一侧区段而与端口p1相连。电磁波施加部13隔着波导管12的另一侧区段而与端口p2相连。在端口p3处,设有虚设负载182。
[0177]
磁铁所形成的磁场与穿透循环器181的电磁波发生相互作用,从而进入端口p1的电磁波会从端口p2射出,而进入端口p2的电磁波会从端口p3射出。因此,循环器181将电磁波产生部11产生的电磁波耦合到前往电磁波施加部13的方向上,并且将电磁波施加部13的内部空间中反射过来的电磁波耦合到虚设负载182。
[0178]
虚设负载182由吸收2.45ghz频率的电磁波的材料构成。因此,虚设负载182吸收从电磁波施加部13的内部空间反射过来的电磁波,并将电磁波能量转换为热量。
[0179]
虚设负载182中设有冷却管183。冷却管183的内部采用供冷却后的冷媒(例如水、空气)进行循环的构造。由于冷却后的冷媒可以从虚设负载182带走热量,因此可以防止虚设负载182的温度过度上升。
[0180]
如上述那样构成的循环器181能够以几乎无损耗的方式将电磁波产生部11产生的电磁波耦合到电磁波施加部13,并且能够吸收在电磁波施加部13的内部空间中反射的电磁波。也就是说,循环器181能够以几乎无损耗的方式从电磁波产生部11向容器14传播电磁波,并且能够吸收从容器14向电磁波产生部11传播的电磁波。因此,能够抑制:因从电磁波施加部13的内部空间反射过来的电磁波返回到电磁波产生部11而对电磁波产生部11的工作产生不良影响。
[0181]
(电磁波施加部)
[0182]
电磁波施加部13是内部空间中空的金属制箱状构件,并且构成为能够在其内部空间中容纳容器14。电磁波施加部13使从波导管12的另一端入射进来的电磁波施加到容器14以及容纳在容器14中的加热对象物。电磁波施加部13构成为将电磁波限制在内部空间中而使其不易泄漏到外部。
[0183]
(容器)
[0184]
容器14是形成为皿状的容器。容器14的形状只要是能够容纳起始物料与氢氧化钠的粉末状混合物m
p
,则无限定。但容器14优选具有较大的开口部,以便使用后述温度计17测量粉末状混合物m
p
的温度。此外,加热工序s13之后若直接使用容器14来实施溶解工序s14,
则优选容器14具有能够容纳规定量的盐酸溶液的容积。
[0185]
此外,若是如后述实施例那样使用研钵将起始物料的粉末与氢氧化钠(后述实施例中为氢氧化钠粉末)混合来获得粉末状混合物,那么该研钵发挥混合部的功能。此外,若是将起始物料粉末和氢氧化钠粉末放入容器14中并在容器14中混合它们来获得粉末状混合物,那么容器14发挥混合部的功能。
[0186]
容器14优选由相对于电磁波产生部11产生的电磁波(在本实施方式中为2.45ghz)表现为高透过率的材料构成。此外,容器14优选由相对于酸和碱呈高耐受性的材料构成。若容器14由相对于酸和碱呈高耐受性的材料构成,就能够在实施加热工序s13之后通过将盐酸溶液倒入容器14来实施溶解工序s14。
[0187]
在本实施例中,容器14由以聚四氟乙烯为代表的氟系树脂构成。但构成容器14的材料不限是氟系树脂,也可以是以聚醚醚酮为代表的芳香族聚醚酮树脂,还可以是聚酰亚胺树脂,还可以是以氧化铝和氧化钛等为代表的氧化物。
[0188]
(旋转台)
[0189]
旋转台15是设置在电磁波施加部13内部空间的底面上的物料台,其构成能在其顶面载置容器14。放平俯视时,旋转台15为圆形,其构成为以其中心轴为旋转轴来以规定的速度进行旋转。根据该结构,载置在旋转台15的顶面上的容器14可周期性地旋转,因此可以更均匀地加热粉末状混合物m
p
。
[0190]
(搅拌子)
[0191]
搅拌子16是设置在电磁波施加部13内部空间的天花板上的金属制旋翼状构件。其通过与旋翼状构件的中心连结着的支撑杆,以能自由旋转的状态固定在所述天花板上。搅拌子16以支撑杆为旋转轴来以规定的速度进行旋转,从而反射由电磁波产生部11产生的电磁波,并使散射在电磁波施加部13的内部空间中。根据该结构,搅拌子16使电磁波散射,因此可以更均匀地加热粉末状混合物m
p
。
[0192]
(温度计)
[0193]
温度计17是辐射温度计,其通过检测粉末状混合物m
p
辐射的红外线来测量容器14的温度。温度计17以能够通过其光接收部来检测来自粉末状混合物m
p
的红外线的方式,固定在电磁波施加部13侧壁的局部。温度计17向控制部输出温度信号,该温度信号表示所测得的粉末状混合物m
p
的温度。
[0194]
(控制部)
[0195]
控制部可以控制电磁波产生部11的功率输出,以使该功率输出达到规定值。控制部还可以以从温度计17收到的温度信号所示的温度达到预定温度的方式,控制电磁波产生部11的功率输出。予以说明,这些预定温度既可以在时间轴上恒定,也可以按照时间来变化。在本实施例中,控制部控制电磁波产生部11将功率输出的值控制成按照时间来变化。功率输出的控制模式的一个例子是将300w的功率输出维持600秒,然后将功率输出控制成0w。
[0196]
以制造方法m10为例,能采用上述方案的介电加热装置10,将粉末状混合物m
p
容纳在容器14的内部空间中来实施加热工序s13。另外,能通过向实施了加热工序s13后的容器14中注入盐酸溶液,来实施溶解工序s14。此外,若使用介电加热装置10来实施溶解工序s14,由于可以对盐酸溶液进行加热,因此能促进液状混合物在盐酸溶液中的溶解。液状混合物的盐酸溶液是无机物溶液的一个例子。
[0197]
[第1实施例]
[0198]
结合图6,对使用上述介电加热装置10时的制造方法m10的第1实施例进行说明。图6是示出上述加热工序s13的示例中的混合物m的温度变化的图表。在本实施例中,使用绿柱石作为起始物料。
[0199]
本实施例中,在粉碎
·
混合工序s12中使用球磨机粉碎了绿柱石。实施了粉碎
·
混合工序s12后的绿柱石的粒径为150μm以下。另外,用研钵粉碎了氢氧化钠30分钟。在此基础上,分别取0.2g绿柱石的粉末和2g氢氧化钠的粉末,用研钵混合,得到了粉末状混合物m
p
。
[0200]
本实施例中,在加热工序s13中将粉末状混合物m
p
置于氧化铝(alumina;al2o3)制的容器14上,用介电加热装置10在大气气氛、常压下进行了介电加热。将介电加热装置10的功率输出值设定为300w,将加热时间设定为8分钟。通过实施加热工序s13,粉末状混合物m
p
随着介电加热而熔解,8分钟后全部成为乳液状的液状混合物。下文中,如果不需要区分混合物是粉末状还是液状,则简称为混合物m。在本实施例的加热工序s13中,混合物m的最高到达温度约为220℃。
[0201]
另外,功率输出值设定为300w后,混合物m的温度在从0秒到约345秒的期间持续显示为50℃。这是因为温度计17的可检测温度的下限起始值是50℃的缘故。
[0202]
本实施例中,液状混合物冷却至常温后,在溶解工序s14中于大气气氛、室温和常压下将液状混合物加入盐酸水溶液(hcl;6mol/l,20cm3)中。其结果,液状混合物完全溶解在了盐酸水溶液中(确认到有99%的铍得以溶解)。
[0203]
[第2实施例]
[0204]
以下说明使用上述介电加热装置10时的制造方法m10的第2实施例。在本实施例中,将锂矿石的一例即锂辉石用作起始物料(spodumene;lialsi2o6)。
[0205]
本实施例中,在粉碎
·
混合工序s12中使用球磨机粉碎了锂辉石。实施了粉碎
·
混合工序s12后的锂辉石的粒径为150μm以下。另外,用研钵粉碎了氢氧化钠30分钟。在此基础上,分别取0.2g锂辉石的粉末和2g氢氧化钠的粉末,用研钵混合,得到粉末状混合物m
p
。
[0206]
本实施例中,在加热工序s13中将粉末状混合物m
p
置于氧化铝(氧化铝:al2o3)制的容器14上,用介电加热装置10在大气气氛、常压下进行了介电加热。介电加热带来的温度履历与图6的趋势相同。将介电加热装置10的功率输出值设定为300w,将加热时间设定为8分钟。通过实施加热工序s13,粉末状混合物m
p
随着介电加热而熔解,8分钟后全部成为乳液状的液状混合物。下文中,如果不需要区分混合物是粉末状还是液状,则简称为混合物m。在本实施例的加热工序s13中,混合物m的最高到达温度约为220℃。
[0207]
本实施例中,液状混合物冷却至常温后,在溶解工序s14中于大气气氛、室温和常压下将液状混合物加入盐酸水溶液(hcl;6mol/l,20cm3)中。其结果,液状混合物溶解在了盐酸水溶液中(确认到有90%以上的锂得以溶解)。
[0208]
(参考例)
[0209]
此外,作为制造方法m10中的加热工序s13的参考例,进行了氢氧化钠粉末的介电加热和碳酸氢钠粉末的介电加热。结合图7和图8来对结果进行说明。图7示出了对氢氧化钠粉末进行介电加热后所得到的结果,是氢氧化钠的温度变化的图表。图8示出了对碳酸氢钠粉末进行介电加热后所得到的结果,是碳酸氢钠的温度变化的图表。
[0210]
以与上述实施例同样的方式,使用研钵将氢氧化钠及碳酸氢钠各自粉碎了30分
钟。在此基础上,分别取2g氢氧化钠和2g碳酸氢钠,并使用介电加热装置10对它们进行了介电加热。在本参考例中,将介电加热装置10的功率输出值设定为300w,将加热时间设定为10分钟。
[0211]
结合图7可知,通过实施介电加热,氢氧化钠粉末被加热,其最高到达温度约为250℃。实施此介电加热后的氢氧化钠熔解为液状。根据该结果,认为粉末状混合物m
p
中的氢氧化钠在制造方法m10的加热工序s13中吸收了用于介电加热的电磁波的能量。
[0212]
另一方面,结合图8可知,即使在实施介电加热的情况下,碳酸钠粉末的温度也几乎不会上升。在图8中,碳酸钠的温度低于50℃,即低于温度计17的可检测温度的下限起始值。根据该结果,认为已知的现有碱熔融法中采用的碳酸钠几乎不吸收用于介电加热的电磁波的能量。
[0213]
另外,虽然图表未示出,但发现只对绿柱石及锂辉石中的至少一种粉末进行介电加热时,绿柱石及锂辉石中的至少一种粉末与碳酸钠粉末的情况相同地,温度几乎不会上升。根据该结果,认为未与氢氧化钠混合的绿柱石及锂辉石几乎不吸收用于介电加热的电磁波的能量。
[0214]
[第7实施方式]
[0215]
《铍的制造系统》
[0216]
结合图9及图10对本发明第7实施方式的铍的制造系统20进行说明。图9是用于制造铍溶液(becl2溶液)的制造装置20a的示意图,该制造装置20a构成铍的制造系统20的一部分。图10的(a)是结晶装置20b、去水化装置20c及电解装置20d的示意图。图10的(b)是图10的(a)所示结晶装置20b所具备的结晶处理槽31的变形例的示意图。图10的(c)是图10的(a)所示去水化装置20c所具备的干燥机33的变形例的示意图。结晶装置20b、去水化装置20c及电解装置20d分别构成铍的制造系统20的一部分。在下文中,也将铍的制造系统20简称为制造系统20,将铍溶液的制造装置20a简称为制造装置20a。
[0217]
如图9和图10所示,制造系统20具备制造装置20a、结晶装置20b、去水化装置20c和电解装置20d。制造系统20是用于实施图2的(a)所示制造方法m20的装置。更具体地,制造装置20a是用于实施图1所示制造方法m10中的除了取出工序s11之外的各工序的装置。结晶装置20b和去水化装置20c是用于实施图2的(a)所示去水化工序s21的装置。电解装置20d是用于实施图2的(a)所示电解工序s22的装置。
[0218]
在本实施方式中,与第1实施方式同样地,将氚增殖材料的一例即钛酸锂(li2tio3)、以及中子倍增材料的一例即铍(be)用作起始物料,其中该铍(be)的表面上形成有由氧化铍(beo)构成的氧化层。但是,制造装置20a中的起始物料不限为如第1实施方式所示那样的钛酸锂(li2tio3)、及表面上形成有由氧化铍(beo)构成的氧化层的铍(be)。
[0219]
(铍溶液的制造装置20a)
[0220]
如图9所示,制造装置20a具备粉碎器21a、进料器f1a、粉碎器21b、进料器f1b、阀v1~v15、介电加热装置22、过滤器23、29、容器24、26、27、28、30及离心机25。另外,制造装置20a具备图9中未示出的控制部。控制部分别控制进料器f1a和f1b、阀v1~v15及介电加热装置22。
[0221]
粉碎器21a将作为起始物料所投入过来的钛酸锂及表面上形成有氧化层的铍粉碎成粉末。在此基础上,粉碎器21a将钛酸锂粉末和铍粉末供给到进料器f1a。粉碎器21a可以
根据期望的规格来从现有粉碎器中适当地选择。因此,这里省略有关粉碎器21a的详细说明。通过使用粉碎器21a来粉碎起始物料,即使中子倍增材料的一例即铍的表面上形成有氧化层,也可以机械地破坏该氧化层来使覆盖在氧化层下的铍暴露。因此,可以提高加热工序s13中将铍及氢氧化钠一同熔解的速度。
[0222]
进料器f1a由控制部控制,从而将从粉碎器21a供给过来的起始物料供给到后述介电加热装置22的容器22c。进料器f1a是用于向容器22c供给起始物料的原料供给部的示例。
[0223]
粉碎器21b将投入过来的氢氧化钠粉碎成粉末。在此基础上,粉碎器21b将氢氧化钠粉末供给到进料器f1b。粉碎器21b可以根据期望的规格来从现有粉碎器中适当地选择。因此,这里省略有关粉碎器21b的详细说明。通过使用粉碎器21b来粉碎氢氧化钠,可以将氢氧化钠的粒径调节到所需的尺寸。如上所述,氢氧化钠的形状不限于粉末。因此,在制造装置20a中也可以省略粉碎器21b。
[0224]
进料器f1a由控制部控制,从而将从粉碎器21a供给过来的起始物料的粉末供给到后述介电加热装置22的容器22c。进料器f1a是用于向容器22c供给起始物料的原料供给部的示例。同样地,进料器f1b由控制部控制,从而将从粉碎器21b供给过来的氢氧化钠粉末供给到后述介电加热装置22的容器22c。进料器f1b是用于向容器22c供给氢氧化钠的氢氧化物供给部的示例。
[0225]
介电加热装置22具备电磁波产生部22a、波导管22b、容器22c、搅拌机构和温度计。介电加热装置22实施图1所示制造方法m10中的加热工序s13和溶解工序s14。
[0226]
电磁波产生部22a由控制部控制,从而产生具有规定频率的电磁波。规定频率例如可以在微波频带内适当选择,但在本实施方式中,采用2.45ghz作为规定频率。2.45ghz的频率与家用微波炉中采用的电磁波频率相同。
[0227]
波导管22b是金属制圆柱形构件,其一端连接到电磁波产生部22a,另一端连接到容器22c。波导管22b将电磁波产生部22a产生的电磁波,从波导管22b的一个端传导到波导管22b的另一端,并且将该电磁波从波导管22b的另一端辐射到容器22c的内部空间。虽然在图9中未示出,但是在波导管22b的中途区段设有图5所示的隔离器。在这种情况下,将图5所示的波导管12理解为波导管22b即可。
[0228]
容器22c是用于在其内部空间中容纳起始物料粉末和氢氧化钠粉末的箱状构件。容器22c与图4所示的容器14同样地由耐酸性的材料构成。从粉碎器21a经由进料器f1a供给过来的起始物料粉末、和从粉碎器21b经由进料器f1b供给过来的氢氧化钠粉末被供给到容器22c。在容器22c的内部,设置有图9中未示出的搅拌机构。控制部使搅拌机构旋转,从而将供给到容器22c内部空间的起始物料粉末和氢氧化钠粉末混合成粉末状混合物。如此,容器22c是用以将起始物料粉末和氢氧化钠粉末混合来获得粉末状混合物的混合部的示例。容器22c也可以是诸如回转窑炉那样的绕轴旋转的管状容器。另外,通过将回转窑炉与后述液体供给部组合,就能实施连续处理。
[0229]
图9中未示出的温度计对容纳在容器22c内部空间中的内容物(此时为粉末状混合物)的温度进行检测,并将表示该温度的温度信号输出到控制部。温度计可以是非接触式温度计,如辐射温度计,也可以是接触式温度计,如热电偶。无论采用何种方式的温度计,温度计均优选设置在容器22c的内部空间,并且构成为能够直接检测容纳在该内部空间中的内容物的温度。
[0230]
控制部可以控制电磁波产生部22a的功率输出,以使该功率输出达到规定值。控制部还可以以从温度计收到的温度信号所示的温度达到预定温度的方式,控制电磁波产生部22a的功率输出。予以说明,这些预定温度既可以在时间轴上恒定,也可以按照时间来变化。在本实施方式中,控制部控制电磁波产生部22a的功率输出,以使得温度信号所示的温度以预定计划来按照时间进行变化。作为温度预定计划的一个例子,可以举出如下模式:花费5分钟来从室温变为250℃,然后在250℃下维持10分钟。
[0231]
如此构成的介电加热装置22通过实施图1所示制造方法m10中的加热工序s13,来获得含有起始物料和氢氧化钠的液状混合物。
[0232]
接下来,经由阀v1来供给hcl溶液。经由该阀v1将hcl溶液供给到容器22,从而实施溶解工序s14。关于经由该阀v1将hcl溶液供给到容器22的机构,其作为向液状混合物供给酸性溶液的液体供给部来发挥功能。在容器22c中,液状混合物溶解于hcl溶液,从而成为含锂的铍溶液(becl2溶液)。如上所述,将含有起始物料和氢氧化钠的液态混合物溶解的液体并不限是hcl溶液等酸溶液,也可以是水。若使用水作为该液体,则是经由阀v1将水供给到容器22c来实施溶解工序s14。
[0233]
在溶解工序s14的实施过程中,控制部也可以控制电磁波产生部22a的功率输出,使得该功率输出达到规定值,控制部还可以以从温度计收到的温度信号所示的温度达到预定温度的方式,控制电磁波产生部22a的功率输出。通过在溶解工序s14的实施过程中实施介电加热,可促进液状混合物相对于hcl溶液的溶解。此外,在溶解工序s14的实施过程中,控制部也可以使搅拌机构持续工作。
[0234]
阀v2使容器22c内部空间与后述过滤器23之间的路径打开或关闭。控制部在加热工序s13及溶解工序s14的实施过程中始终关闭阀v2,并且在加热工序s13及溶解工序s14的实施后打开阀v2。其结果,经加热工序s13而得的含锂的铍溶液便从容器22c供给到过滤器23。
[0235]
过滤器23使含锂的铍溶液之中的液相(即,含有licl的becl2溶液)滤过,并滤阻该铍溶液之中的固相(即,氧化钛)。即,过滤器23实施制造方法m10中的第1过滤工序s15。过滤器23可以根据期望的规格来从现有过滤器中适当地选择。因此,这里省略有关过滤器23的详细说明。
[0236]
阀v3使过滤器23与后述容器24之间的路径打开或关闭。控制部至少在含锂的铍溶液被供给至过滤器23的过程中始终打开阀v3。其结果,经第1过滤工序s15而得的含有licl的becl2溶液便从过滤器23供给到容器24。
[0237]
容器24是内部空间中空且具有耐酸性及耐碱性的箱状构件。关于容器的构造,下面说明的容器26、27、28和30分别是具有耐酸性的箱状构件。naoh溶液经由阀v4来供给到容器24。关于经由该阀v4将naoh溶液供给至容器24内的铍溶液的机构,其作为向铍溶液供给naoh溶液的naoh溶液供给部来发挥功能。
[0238]
供给到了容器24的含有licl的becl2溶液、及naoh溶液在容器24的内部空间中混合。也就是说,在容器24的内部空间中实施制造方法m10中的氢氧化钠添加工序s16。其结果,在容器24的内部,生成作为固相的氢氧化铍(be(oh)2),而作为液相的lioh溶解到naoh溶液中。
[0239]
虽然在图9中未示出,但容器24的内部空间中也可以设置用于搅拌含有licl的
becl2溶液、及naoh溶液的搅拌机构。同样地,后述容器26、27、28、30的内部空间中也可以设置搅拌机构。
[0240]
阀v5使容器24的内部空间与后述离心机25之间的路径打开或关闭。控制部在氢氧化钠添加工序s16的实施过程中始终关闭阀v5,并且在氢氧化钠添加工序s16的实施后打开阀v5。其结果,经氢氧化钠添加工序s16而得的含有be(oh)2及lioh的naoh溶液便从容器24供给到离心机25。
[0241]
离心机25用于将含有be(oh)2及lioh的naoh溶液之中的液相(即,含有lioh的naoh溶液)与固相(即,be(oh)2)彼此分离。即,离心机25实施制造方法m10中的第2过滤工序s17。离心机25可以根据期望的规格来从现有离心机中适当地选择。因此,这里省略有关离心机25的详细说明。经第2过滤工序s17而得的be(oh)2被投入到后述容器26的内部空间,经第2过滤工序s17而得的含有lioh的naoh水溶液被回收到图中未示出的回收管线。
[0242]
此外,为了将含有be(oh)2及lioh的naoh溶液之中的液相与固相彼此分离,也可以使用诸如过滤器23的过滤器来代替离心机25。
[0243]
hcl溶液经由阀v6来供给到容器26。供给到容器26的be(oh)2及hcl溶液在容器26的内部空间中混合。也就是说,在容器26的内部空间中实施制造方法m10中的盐酸添加工序s18。其结果,在容器26的内部,得到由所生成出的becl2溶解在hcl溶液中而成的铍溶液(becl2溶液)。
[0244]
阀v7使容器26的内部空间与后述容器27的内部空间之间的路径打开或关闭。控制部在盐酸添加工序s18的实施过程中始终关闭阀v7,并且在盐酸添加工序s18的实施后打开阀v7。其结果,经盐酸添加工序s18而得的铍溶液便从容器26供给到容器27。
[0245]
有机化合物溶液经由阀v8来供给到容器27。关于经由该阀v8将有机化合物溶液供给至容器27的机构,其作为向氯化铍溶液供给有机化合物溶液的有机化合物溶液供给部来发挥功能。该有机化合物溶液是制造方法m10的第1杂质去除工序s19中记载的有机化合物溶液。因此,这里省略有关有机化合物溶液的说明。
[0246]
供给到容器27的铍溶液及有机化合物溶液在容器27的内部空间中混合。即,在容器27的内部空间内实施第1杂质去除工序s19。其结果,在容器27的内部,分离得到2个层,即第1元素含量得以抑制了的铍溶液以及含有第1元素的有机化合物溶液。铍溶液的比重大于有机化合物溶液的比重,因此铍溶液位于有机化合物溶液下方。
[0247]
阀v9使容器27的内部空间与回收管线(图中未示出)之间的路径打开或关闭。阀v10使容器27的内部空间与后述容器28的内部空间之间的路径打开或关闭。
[0248]
控制部在第1杂质去除工序s19的实施过程中始终关闭阀v9、v10。在第1杂质去除工序s19的实施后,控制部首先仅打开阀v10。这样,经第1杂质去除工序s19而得的第1元素含量得以抑制了的铍溶液便从容器27供给到容器28。之后,控制部关闭阀v10并打开阀v9。由此,经第1杂质去除工序s19而得的、含有第1元素的有机化合物溶液便被回收到回收管线中。
[0249]
碳酸氢钠经由阀v11来供给到容器28。关于经由该阀v11将碳酸氢钠供给至容器28的机构,其作为向氯化铍溶液供给碳酸氢钠的碳酸氢钠供给部来发挥功能。该碳酸氢钠是制造方法m10的第2杂质去除工序s20中记载的碳酸氢钠。因此,这里省略有关碳酸氢钠的说明。
[0250]
供给到容器28的铍溶液和碳酸氢钠在容器28的内部空间中混合。即,在容器28的内部空间中实施第2杂质去除工序s20。其结果,在容器28的内部,第2元素的氢氧化物得以沉淀,氢氧化铍(be(oh)2)溶液中的第2元素的含量得以抑制。
[0251]
阀v12使容器28的内部空间与后述过滤器之间的路径打开或关闭。控制部在第2杂质去除工序s20的实施过程中始终关闭阀v12,并且在第2杂质去除工序s20的实施后打开阀v12。其结果,经第2杂质去除工序s20而得的含有第2元素氢氧化物的氢氧化铍溶液便从容器28供给到过滤器29。
[0252]
过滤器29使含有第2元素氢氧化物的氢氧化铍溶液之中的液相(即,氢氧化铍溶液)滤过,并滤阻该氢氧化铍溶液之中的固相(即,第2元素的氢氧化物)。过滤器29可以根据期望的规格来从现有过滤器中适当地选择。因此,这里省略有关过滤器29的详细说明。
[0253]
阀v13使过滤器29与后述容器30之间的路径打开或关闭。控制部至少在含有第2元素氢氧化物的氢氧化铍溶液被供给至过滤器29的过程中始终打开阀v13。其结果,经第2杂质去除工序s20而得的第2元素含量得以抑制了的氢氧化铍溶液便从过滤器29供给到容器30。
[0254]
氢氧化铍溶液经由来阀v13供给到容器30,hcl溶液经由阀v14来供给到容器30。供给到容器30的be(oh)2溶液和hcl溶液在容器30的内部空间中混合。其结果,在容器30的内部,得到由所生成出的becl2溶解在hcl溶液中而成的铍溶液(becl2溶液)。
[0255]
阀v15使容器30与后述结晶装置20b的结晶处理槽31之间的路径打开或关闭。控制部至少在hcl溶液被供给至容器30的过程中始终关闭阀v15,并且在供给到容器30的be(oh)2溶液和hcl溶液完成了充分混合后,打开阀v15。其结果,铍溶液(becl2溶液)便从容器30供给到结晶处理槽31。
[0256]
(结晶装置20b)
[0257]
如图10的(a)所示,结晶装置20b具备结晶处理槽31、冷却器c、泵p、冷凝槽和阀v16、v17。此外,结晶装置20b具备图10的(a)中未示出的控制部。控制部分别控制结晶处理槽31、冷却器c、泵p、阀v16和v17。
[0258]
结晶处理槽31包括内侧槽和外侧槽。热水经由阀v16来供给到外侧槽的内部空间。由制造装置20a生成的铍溶液(becl2溶液)被供给到内侧槽的内部空间。上述热水用来加热容纳在内侧槽中的铍溶液和hcl溶液。利用热水的这一手法是采用外部加热方式的加热手段的示例。
[0259]
冷却器c、冷凝槽和泵p构成减压脱水系统。泵p对内侧槽的内部空间进行抽气。冷却器c冷却从内侧槽的内部空间抽出的气体。冷凝槽储存由冷却器c冷却而液化了的冷凝水。
[0260]
如此配置的结晶装置20b可以使氯化铍结晶。结晶了的氯化铍经由阀v17而从结晶处理槽31供给到后述离心机32。
[0261]
结晶处理槽31也可以具备如图10的(b)所示的电磁波产生部31a和波导管31b,来替代供给热水的阀v16。电磁波产生部31a和波导管31b分别与图9所示的电磁波产生部22a和波导管22b以同样的方式构成,并且是介电加热装置的示例。
[0262]
如上所述,结晶装置20b中用于加热铍溶液和hcl溶液的加热手段可以是如图10的(a)所示的外部加热方式,也可以是如图10的(b)所示的介电加热方式。从能效的角度来看,
优选采用介电加热方式。
[0263]
(去水化装置20c)
[0264]
如图10的(a)所示,去水化装置20c具备离心机32和干燥机33。另外,去水化装置20c具备图10的(a)中未示出的控制部。控制部分别控制离心机32及干燥机33。
[0265]
经结晶装置20b而结晶了的氯化铍通过离心机32来得以脱水。脱水了的氯化铍通过干燥机33来得以去水化。作为干燥机33,可举出生成热风的热风生成机构,利用由该热风生成机构生成的热风来加热氯化铍,从而将其去水化。即,结晶装置20b和去水化装置20c是本发明中所述的去水化装置的示例,且可以用来实施图2所示制造方法m20中的去水化工序s21。热风是采用外部加热方式的加热手段的示例。
[0266]
另外,干燥机33也可以具备电磁波产生部33a和波导管33b(见图10的(c)),来替代产生热风的热风产生机构。电磁波产生部33a和波导管33b分别与图9所示的电磁波产生部22a和波导管22b以同样的方式构成,并且是介电加热装置的示例。
[0267]
如上所述,去水化装置20c中用于加热氯化铍的加热手段可以是如图10的(a)所示的外部加热方式,也可以是如图10的(c)所示的介电加热方式。另外,从能效的角度来看,优选采用介电加热方式。
[0268]
(电解装置20d)
[0269]
如图10的(a)所示,电解装置20d具备电解炉34a、电源34b、阳极34c、阴极34d和进料器f2。另外,电解炉34a具备图10的(a)中未示出的加热器。另外,电解装置20d具备图10的(a)中未示出的控制部。控制部分别控制电源34b、加热器和进料器f2。
[0270]
由去水化装置20c生成了的去水化的氯化铍供给到电解炉34a的炉内。此外,氯化钠(nacl)经由进料器f2供给到电解炉34a的炉内。
[0271]
炉内容纳有氯化铍和氯化钠的电解炉34a采用加热器来进行加热。其结果,氯化铍和氯化钠得以熔融。另外,通过使用在氯化铍中添加氯化钠而成的双成分浴来作为电解浴,可以降低电解浴的熔点。加热时的电解炉34a的温度可以适当地在超过上述双成分浴熔点的范围内选定。作为电解炉34a的温度的例子,可以举出350℃。
[0272]
阳极34c例如是由碳制成的电极,阴极34d例如是由镍制成的电极。
[0273]
在上述双成分浴的熔融状态下,控制部采用电源34b来使电流流过阳极34c与阴极34d之间。结其果,上述双成分浴被电解,从而在阴极34d的表面上生成金属铍。
[0274]
如上所述,电解装置20d能够实施图2所示制造方法m20中的电解工序s22。
[0275]
[其他实施方式]
[0276]
在上述第7实施方式中,对采用了制造装置20a、结晶装置20b及去水化装置20c来实施制造方法m20的制造系统20、即铍的制造系统20进行了说明。
[0277]
然而,本发明的范畴不仅包括铍的制造系统20,还包括用于实施氢氧化铍制造方法m30的氢氧化铍制造系统、及用于实施氧化铍制造方法m40的氧化铍制造系统。
[0278]
氢氧化铍制造系统具备图9所示制造装置20a、以及中和装置。该中和装置通过用碱来中和由制造装置20a生成的氯化铍溶液,从而生成氢氧化铍。例如,中和装置可以由分别与图9所示的容器24、阀v4、v5以及离心机25同等的各部件所构成。此外,作为用于中和的碱,也可采用氨来替代氢氧化钠。
[0279]
氧化铍制造系统具备图9所示制造装置20a、以及第3加热装置。该第3加热装置通
过加热由制造装置20a生成的氯化铍溶液来生成氧化铍。第3加热装置没有限定,例如可以使用电炉。
[0280]
另外,在“(铍溶液制造方法的变形例)”栏目及“(锂溶液制造方法)”栏目中,说明了在将铍矿石(例如绿柱石)或锂矿石(例如锂辉石)用作起始物料的情况下,可以省略氢氧化钠添加工序s16、第2过滤工序s17及盐酸添加工序s18。因此,在使用制造装置20a且将铍矿石或锂矿石用作起始物料的情况下,可以省去用以实施氢氧化钠添加工序s16、第2过滤工序s17及盐酸添加工序s18的各结构。即,将从阀v3供给过来的、经第1过滤工序s15而得的铍溶液或锂溶液,直接供给到容器27即可。
[0281]
[第8实施方式及第9实施方式]
[0282]
结合图11,说明本发明第8实施方式的氢氧化锂(lioh)制造方法m70和本发明第9实施方式的碳酸锂(li2co3)制造方法m80。图11的(a)和(b)分别是氢氧化锂制造方法m70及碳酸锂制造方法m80的流程图。
[0283]
氢氧化锂制造方法m70及碳酸锂制造方法m80中均使用经第2过滤工序s17而分离出的含氢氧化锂的作为液相的溶液。此外,可以根据当时的优先级,适当地决定要实施氢氧化锂制造方法m70及碳酸锂制造方法m80中的哪一种。
[0284]
(氢氧化锂制造方法m70)
[0285]
如图11的(a)所示,氢氧化锂制造方法m70包括干燥工序s71。干燥工序s71是使经第2过滤工序s17而分离出的溶液蒸发并且将析出的氢氧化锂干燥的工序。通过实施氢氧化锂制造方法m70,可以获得固体氢氧化锂。
[0286]
(碳酸锂制造方法m80)
[0287]
如图11的(b)所示,碳酸锂制造方法m80包括二氧化碳气导入工序s81、第4过滤工序s82和干燥工序s83。
[0288]
二氧化碳气导入工序s81是向经第2过滤工序s17而分离出的溶液中导入二氧化碳从而在溶液中沉淀出碳酸锂的工序。
[0289]
第4过滤工序s82是在二氧化碳气导入工序s81之后实施的工序。第4过滤工序s82是使用过滤器将沉淀在溶液中的碳酸锂从溶液中分离的工序。
[0290]
干燥工序s83是在第4过滤工序s82之后实施的工序。干燥工序s83是将经第4过滤工序s82而分离出的碳酸锂干燥的工序。
[0291]
通过实施碳酸锂制造方法m80,能获得固体碳酸锂。
[0292]
(小结)
[0293]
如上所述,通过使用经第2过滤工序s1分离出的含氢氧化锂的作为液相的溶液,来实施氢氧化锂制造方法m70或碳酸锂制造方法m80,能够制造固体的氢氧化锂或碳酸锂。因此,能将经第2过滤工序s17而分离出的作为液相的氢氧化锂,作为资源来回收而不浪费。
[0294]
予以说明,与分离方法m50的情况同样地,氢氧化锂制造方法m70及碳酸锂制造方法m80分别能与制造方法m10的一部分进行组合。
[0295]
[第10实施方式]
[0296]
结合图12,说明本发明第10实施方式的碳酸锂(li2co3)制造方法m90。图12是制造方法m90的流程图。在本实施方式中,将锂矿石的一例即锂辉石(spodumene;lialsi2o6)用作起始物料。
[0297]
如图12所示,制造方法m90包括粉碎
·
混合工序s12、加热工序s13、溶解工序s14、第1过滤工序s15、氢氧化钠添加工序s16、第2过滤工序s17、二氧化碳气导入工序s91、分离工序s92、干燥工序s93。
[0298]
关于制造方法m90中的粉碎
·
混合工序s12~第2过滤工序s17,除了起始物料是锂辉石的这一点以外,与制造方法m10中的粉碎
·
混合工序s12~第2过滤工序s17同样。因此,在本实施方式中,省略对粉碎
·
混合工序s12~第2过滤工序s17的详细说明。
[0299]
在本实施方式中,将氢氧化钠(naoh)用作在粉碎
·
混合工序s12中与起始物料混合的氢氧化物,并且将盐酸用作在溶解工序s14中使用的酸溶液。
[0300]
通过实施溶解工序s14,能获得酸溶液,该酸溶液含有:锂辉石中所含的锂、铝、硅的各自的离子;以及氯化钠(nacl)。
[0301]
通过实施第1过滤工序s15,能够将固相中所含的硅酸(h2sio3)分离。
[0302]
另外,通过实施氢氧化钠添加工序s16和第2过滤工序s17,能够将固相中所含的氢氧化铝(al(oh)3)分离。此外,当起始物料中存在微量的铁(fe)时,能够将固相中所含的铁以氢氧化铁(fe(oh)3)的方式分离。其结果,能得到含有氢氧化锂(lioh)及氯化钠(nacl)的氢氧化钠溶液。
[0303]
二氧化碳气导入工序s91与图11的(b)所示碳酸锂制造方法m80中的二氧化碳气导入工序s81同样。因此,在本实施方式中,省略二氧化碳气导入工序s91的说明。通过实施二氧化碳气导入工序s91,能获得含有碳酸锂(li2co3)、氯化钠及碳酸钠(na2co3)的液相。
[0304]
分离工序s92是从含有碳酸锂(li2co3)、氯化钠及碳酸钠(na2co3)的液相中将碳酸钠(na2co3)分离的工序。分离工序s92通过对含有碳酸锂、氯化钠及碳酸钠的液相进行减压浓缩,能够得到分散有碳酸锂的悬浮液。这类悬浮液又称浆液。减压浓缩优选在70℃以下的温度下实施。
[0305]
此外,在分离工序s92中,对上述悬浮液实施离心分离。通过实施离心分离,可以使析出的碳酸锂沉淀。因此,将液相所含的氯化钠及碳酸钠,与固相所含的碳酸锂彼此分离。
[0306]
干燥工序s93与图11的(b)所示碳酸锂制造方法m80中的干燥工序同样。干燥工序s93是将经分离工序s92而分离出的碳酸锂干燥的工序。
[0307]
通过如上述那样实施碳酸锂制造方法m90,能够以锂辉石为起始物料来得到固体碳酸锂。
[0308]
《制造方法m90的变形例》
[0309]
虽然在本实施方式中使用了锂辉石作为起始物料的,但制造方法m90中使用的起始物料不限于锂辉石。作为起始物料,例如可举出氧化物矿(例如铝土矿)和人造复合氧化物(例如氧化钇稳定化型氧化锆(ysz)和堇青石)。铝土矿含有氧化铝水合物(al2o3·
2h2o)和铝(al)。ysz含有氧化锆(zirconium oxide,zro2)和氧化钇(yttrium oxide,y2o3)。堇青石含有氧化镁(mgo)、氧化铝(al2o3)和氧化硅(sio2)。
[0310]
即使在使用这些起始物料的情况下,也可以良好地采用制造方法m90。如制造方法m10的说明所述的,在粉碎
·
混合工序s12中与起始物料混合的氢氧化物可以是氢氧化钠,也可以是氢氧化钾。此外,在溶解工序s14中将液状混合物溶解的液体可以是以盐酸、硫酸、王水等为代表的酸溶液,也可以是水。
[0311]
通过如上述那样实施制造方法m90的一个变形例,能以氧化物矿或复合氧化物为
起始物料来获得:构成氧化物矿或复合氧化物的无机物得以溶解而成的溶液(例如,铝溶液)。当氧化物矿或复合氧化物中含有多种无机物(例如铝、贵金属等)时,能获得两种以上该无机物得以溶解而成的溶液。
[0312]
[第11实施方式]
[0313]
结合图13,对本发明第11实施方式的碳酸锂(li2co3)制造方法m100进行说明。图13是制造方法m100的流程图。在本实施方式中,将锂矿石的一例即锂辉石(spodumene;lialsi2o6)用作起始物料。
[0314]
如图13所示,制造方法m100包括粉碎
·
混合工序s12、加热工序s13、溶解工序s14、第1过滤工序s15、碳酸氢钠添加工序s1006、第5过滤工序s1007、分离工序s1008、干燥工序s1009。
[0315]
制造方法m100中的粉碎
·
混合工序s12~第1过滤工序s15与制造方法m90中的粉碎
·
混合工序s12~第1过滤工序s15同样。因此,在本实施方式中,省略对粉碎
·
混合工序s12~第1过滤工序s15的详细说明。
[0316]
在第1过滤工序s15之后实施的碳酸氢钠添加工序s1006及第5过滤工序s1007对应于制造方法m90中的氢氧化钠添加工序s16及第2过滤工序s17。通过实施碳酸氢钠添加工序s1006及第5过滤工序s1007,能够将固相中所含的氢氧化铝(al(oh)3)分离。此外,当起始物料中存在微量的铁(fe)时,能够将固相中所含的铁以氢氧化铁(fe(oh)3)的方式分离。其结果,能得到含有碳酸锂、氯化钠(nacl)、碳酸钠(na2co3)及碳酸氢钠(nahco3)的氢氧化钠溶液。
[0317]
制造方法m100中的分离工序s1008及干燥工序s1009对应于制造方法m90中的分离工序s92及干燥工序s93。在制造方法m100的分离工序s1008中,对含有碳酸锂、氯化钠(nacl)、碳酸钠(na2co3)及碳酸氢钠(nahco3)的氢氧化钠溶液进行与制造方法m90的分离工序s92同样的减压浓缩和离心分离,从而获得分散有碳酸锂的悬浮液。但分离工序s1008中,在减压浓缩和离心分离时会预先将甲醇添加到氢氧化钠溶液中。由此,能够使水溶性低于氯化钠及碳酸钠的碳酸氢钠溶解到液相中。
[0318]
干燥工序s1009由于与制造方法m90的干燥工序s93相同,因此这里省略其说明。
[0319]
通过如上述那样实施碳酸锂制造方法m100,能够以锂辉石为起始物料来得到固体碳酸锂。
[0320]
[第12实施方式]
[0321]
结合图14,对本发明第12实施方式的氢氧化锂(lioh)制造方法m110进行说明。图14是制造方法m110的流程图。在本实施方式中,将锂矿石的一例即锂辉石(spodumene:lialsi2o6)用作起始物料。
[0322]
如图14所示,制造方法m110包括粉碎
·
混合工序s12、加热工序s13、溶解工序s14、第1过滤工序s15、第3杂质去除工序s1106、第1萃出工序s1107、硫酸添加工序s1108、第2萃出工序s1109、氢氧化钙添加工序s1110、第6过滤工序s1111、分离工序s1112、干燥工序s1113。
[0323]
制造方法m110中的粉碎
·
混合工序s12~加热工序s13与制造方法m10中的粉碎
·
混合工序s12~加热工序s13同样。因此,在本实施方式中,省略取出工序s11~加热工序s13的详细说明。
[0324]
制造方法m110中的溶解工序s14除了所用酸溶液是硫酸(h2so4)的这一点以外,与制造方法m10中的溶解工序s14同样。因此,在本实施方式中,省略对溶解工序s14的详细说明。通过实施溶解工序s14,能获得酸溶液,该酸溶液含有:锂辉石中所含的锂、铝、硅的各自的离子:以及氢氧化钠中的钠(na)离子。
[0325]
通过实施第1过滤工序s15,能够将固相中所含的硅酸(h2sio3)分离。
[0326]
第3杂质去除工序s1106类似于制造方法m10中的第1杂质去除工序s19,但第3杂质去除工序s1106与第1杂质去除工序s19的不同点在于:使用二(2-乙基己基)磷酸(d2ehpa,di-(2-ethylhexyl)phosphoric acid)和磷酸三丁酯(tbp,tri-n-butyl phosphate)的混合物作为有机化合物,以及还向这些有机化合物进一步混合氢氧化钠(naoh)。通过实施第3杂质去除工序s1106,锂被d2ehpa和tbp所吸附。也就是说,锂包含到有机层中。另一方面,铝、硅和钠不被d2ehpa和tbp吸附而包含到水层中。
[0327]
第1萃出工序s1107是从实施第3杂质去除工序s1106而得的溶液中萃出有机层的工序。
[0328]
硫酸添加工序s1108是在实施第1萃出工序s1107而得的有机层中添加硫酸的水溶液的工序。通过实施硫酸添加工序s1108,d2ehpa和tbp所吸附着的锂形成为硫化锂(li2so4),从而从有机层转移到水层中。因此,水层也可以称为含锂的硫酸水溶液。
[0329]
第2萃出工序s1109是从实施硫酸添加工序s1108而得的溶液中萃出含有硫化锂的水层的工序。
[0330]
氢氧化钙添加工序s1110是在实施第2萃出工序s1109而得的水层(含锂的硫酸水溶液)中添加氢氧化钙(ca(oh)2)的工序。通过实施氢氧化钙添加工序s1110,钙形成为硫酸盐即硫酸钙(caso4)而沉淀,锂经离子化而与氢氧根离子一同溶解。
[0331]
第6过滤工序s1111是使用过滤器将经氢氧化钙添加工序s1110而得的含有锂水溶液中所含的固相和液相彼此分离的工序。固相含有硫酸钙。液相含有氢氧根离子以及离子化了的锂。
[0332]
制造方法m110的分离工序s1112和干燥工序s1113对应于制造方法m90的分离工序s92和干燥工序s93。在分离工序s1112中,能对含有氢氧根离子以及离子化了的锂的溶液进行与分离工序s92同样的减压浓缩和离心分离。通过实施分离工序s1112,能获得分散有氢氧化锂的悬浮液。干燥工序s1113由于与制造方法m90的干燥工序s93相同,因此这里省略其说明。
[0333]
通过如上述那样实施氢氧化锂的制造方法m110,能够以锂辉石为起始物料来得到固体氢氧化锂。
[0334]
另外,通过对实施第2萃出工序s1109而得的含硫化锂的水层分别实施与分离工序s1112及干燥工序s1113同样的分离工序及干燥工序,就能得到固体的硫化锂。
[0335]
[第13实施方式]
[0336]
结合图15,对本发明第13实施方式的碳酸锂(li2co3)制造方法m120进行说明。图15是制造方法m120的流程图。在本实施方式中,将锂矿石的一例即锂辉石(spodumene;lialsi2o6)用作起始物料。
[0337]
如图15所示,制造方法m120包括粉碎
·
混合工序s1202、加热工序s1203、溶解工序s1204、第1过滤工序s1205、二氧化碳气导入工序s1206、分离工序s1208、干燥工序s1209。
[0338]
制造方法m120中的粉碎
·
混合工序s1202及加热工序s1203与制造方法m90中的粉碎
·
混合工序s12及加热工序s13同样。因此,在本实施方式中,省略对粉碎
·
混合工序s1202及加热工序s1203的详细说明。
[0339]
溶解工序s1204是将经加热工序s1203而得的液状混合物溶解于水(h2o)的工序。通过实施溶解工序s1204,可以得到溶解有锂(li)和硅(si)且含有析出的氢氧化铝的氢氧化钠水溶液。
[0340]
第1过滤工序s1205是使用过滤器将经溶解工序s1204而得的氢氧化钠水溶液中所含的固相和液相彼此分离的工序。固相含有氢氧化铝。液相是溶解有锂(li)和硅(si)的氢氧化钠水溶液。
[0341]
二氧化碳气导入工序s1206是向经第1过滤工序s1205而分离出的氢氧化钠水溶液中导入二氧化碳气体的工序。通过实施二氧化碳气导入工序s1206,锂和钠分别形成为碳酸盐,即形成为碳酸锂和碳酸钠。硅形成为硅酸根离子。
[0342]
制造方法m120的分离工序s1208及干燥工序s1209对应于制造方法m90的分离工序s92及干燥工序s93。在分离工序s1208中,对含有碳酸锂、碳酸钠和硅酸根离子的溶液进行与分离工序s92同样的减压浓缩和离心分离。通过实施分离工序s1208,能获得分散有碳酸锂的悬浮液。干燥工序s1209由于与制造方法m90的干燥工序s93相同,因此在此省略其说明。
[0343]
通过如上述那样实施碳酸锂的制造方法m120,在以锂辉石为起始物料的情况下,即使在溶解工序s1204中使用水而不使用酸溶液,也能得到固体碳酸锂。
[0344]
[第14实施方式]
[0345]
结合图16,说明本发明第14实施方式的氢氧化锂(lioh)制造方法m130。图16是制造方法m130的流程图。在本实施方式中,将锂矿石的一例即锂辉石(spodumene;lialsi2o6)用作起始物料。
[0346]
如图16所示,制造方法m130包括粉碎
·
混合工序s1202、加热工序s1203、溶解工序s1204、第1过滤工序s1205、第4杂质去除工序s1306、第1萃出工序s1107、硫酸添加工序s1108、第2萃出工序s1109、氢氧化钙添加工序s1110、第6过滤工序s1111、分离工序s1112、干燥工序s1113。
[0347]
制造方法m130中的粉碎
·
混合工序s1202~第1过滤工序s1205与制造方法m120中的粉碎
·
混合工序s1202~第1过滤工序s1205同样。因此,在本实施方式中,省略粉碎
·
混合工序s1202~第1过滤工序s1205的详细说明。
[0348]
第4杂质去除工序s1306类似于制造方法m110中的第3杂质去除工序s1106,但第4杂质去除工序s1306与第3杂质去除工序s1106的不同点在于:使用噻吩甲酰三氟丙酮(tta,thenoyltrifluoroacetone)和磷酸三丁酯(tbp,tri-n-butyl phosphate)的混合物作为有机化合物,以及还向这些有机化合物物进一步混合盐酸(hcl)。通过实施第4杂质去除工序s1306,锂被tta和tbp所吸附。也就是说,锂包含到有机层中。另一方面,铝、硅和钠不被tta和tbp吸附而包含到水层中。
[0349]
制造方法m130中的第1萃出工序s1107~干燥工序s1113与制造方法m110中的第1萃出工序s1107~干燥工序s1113同样。因此,在本实施方式中,省略第1萃出工序s1107~干燥工序s1113的详细说明。
[0350]
通过如上述那样实施氢氧化锂的制造方法m130,在以锂辉石为起始物料的情况下,即使在溶解工序s1204中使用水而不使用酸溶液,也能得到固体氢氧化锂。
[0351]
另外,通过对实施第2萃出工序s1109而得的含硫化锂的水层分别实施与分离工序s1112及干燥工序s1113同样的分离工序及干燥工序,就能得到固体的硫化锂。
[0352]
[第15实施方式]
[0353]
结合图17,对本发明第15实施方式的镍化合物制造方法m140进行说0明。图17是制造方法m140的流程图。在本实施方式中,将镍淤积物用作起始物料。镍淤积物是金属废渣的一种形态,是冶炼镍时产生的矿渣。制造方法m140中能将金属废渣用作起始物料。另外,镍淤积物包含除镍(ni)以外的元素(例如氟(f)或硫(s))。因此,镍淤积物是镍化合物的一个示例。但制造方法m140中可用的起始物料不限是镍淤积物,也可以是在诸如机械或电子部件的制造过程或加工过程等中产生的金属,还也可以是含有这些金属的化合物。
[0354]
在制造方法m140中,并非使镍淤积物中所含的镍溶解到溶液(酸溶液或作为溶剂的水)中,而是使镍以外的元素溶解到溶液中。因此,能通过使镍以外的元素溶解到溶液中来提高以固体方式残留的镍的纯度。因此,制造方法m140也可以称为镍化合物的提纯方法。
[0355]
如图17所示,制造方法m140包括粉碎
·
混合工序s1402、加热工序s1403、溶解工序s1404和第1过滤工序s1405。
[0356]
粉碎
·
混合工序s1402对应于制造方法m10中的粉碎
·
混合工序s12。即,粉碎
·
混合工序s1402是在粉碎起始物料的基础上将起始物料与氢氧化物粉末混合的工序。在本实施方式中,作为氢氧化物,使用了氢氧化钠(naoh)。但氢氧化物不限于氢氧化钠,也可以是氢氧化钾(koh)。粉碎
·
混合工序s1402除了起始物料是镍淤积物的这一点以外,与粉碎
·
混合工序s12同样。因此,在本实施方式中,省略粉碎
·
混合工序s1402的详细说明。
[0357]
加热工序s1403、溶解工序s1404及第1过滤工序s1405分别与制造方法m10中的加热工序s13、溶解工序s14及第1过滤工序s15同样。因此,在本实施方式中,省略加热工序s1403、溶解工序s1404及第1过滤工序s1405的详细说明。
[0358]
在溶解工序s1404中,采用水来作为将经加热工序s1403而得的液状混合物溶解的液体。在本实施方式中,由于液状混合物中所含的氢氧化钠溶于水,因此经溶解工序s1404而得的溶液是含有起始物料的氢氧化钠水溶液。通过实施溶解工序s1404,镍淤积物中所含的氟和硫得以溶解在氢氧化钠中。
[0359]
通过实施第1过滤工序s1405,液相所含的含氟及硫的氢氧化钠溶液便与构成固相的镍淤积物彼此分离。通过回收固相,可以得到相较于作为起始物料时的镍淤积物来看,氟及硫等杂质的浓度得以降低了的镍淤积物。
[0360]
通过如上述那样实施镍化合物的制造方法m140,能够实现镍淤积物的提纯。
[0361]
另外,也可以对实施第1过滤工序s1405而得的固相(即,提纯了1次后的镍淤积物)再次实施制造方法m140。通过两次或更多次返复实施制造方法m140,可以进一步提高获得的镍淤积物中的镍纯度。
[0362]
[第16实施方式]
[0363]
结合图18,对本发明第16实施方式的铁分离方法m150进行说明。图18是分离方法m150的流程图。在本实施方式中,将钨铁矿(fewo4)用作起始物料。钨铁矿是钨酸盐矿物的一个例子。
[0364]
如图18所示,分离方法m150包括粉碎
·
混合工序s1502、加热工序s1503、溶解工序s1504、第1过滤工序s1505、盐酸浸渍工序s1552、第3过滤工序s1553。
[0365]
粉碎
·
混合工序s1502对应于制造方法m10中的粉碎
·
混合工序s12。即,粉碎
·
混合工序s1502是在粉碎起始物料的基础上将起始物料与氢氧化物粉末混合的工序。本实施方式中,氢氧化钠的形状不限于粉末。在本实施方式中,作为氢氧化物,使用了氢氧化钠(naoh)。因此,粉碎
·
混合工序s1502除了起始物料是钨铁矿的这一点以外,与粉碎
·
混合工序s12同样。因此,在本实施方式中,省略粉碎
·
混合工序s1502的详细说明。
[0366]
加热工序s1503、溶解工序s1504及第1过滤工序s1505分别与制造方法m10中的加热工序s13、溶解工序s14及第1过滤工序s15同样。因此,在本实施方式中,省略加热工序s1503、溶解工序s1504及第1过滤工序s1505的详细说明。
[0367]
在溶解工序s1504中,采用水来作为将经加热工序s1503而得的液状混合物溶解的液体。但溶解工序s1504中使用的液体不限于水,也可以是酸溶液(例如盐酸溶液和硫酸溶液)。在本实施方式中,由于液状混合物中所含的氢氧化钠溶于水,因此经溶解工序s1504而得的溶液是含有起始物料的氢氧化钠水溶液。通过实施溶解工序s1504,钨铁矿中所含的钨(w)的大部分(例如90%以上)得以溶解在氢氧化钠中。因此,固相中含有因钨从钨铁矿中溶出而形成的氧化铁。
[0368]
通过实施第1过滤工序s1505,得到构成固相的氧化铁。
[0369]
盐酸浸渍工序s1552及第3过滤工序s1553分别与钛及锂的分离方法m50中的盐酸浸渍工序s52及第3过滤工序s53同样。因此,在本实施方式中,省略盐酸浸渍工序s1552及第3过滤工序s1553的详细说明。
[0370]
通过实施盐酸浸渍工序s1552,氧化铁所含的铁以氯化铁的形式溶解在盐酸溶液中。因此,实施了盐酸浸渍工序s1552后的盐酸溶液的液相中含有氯化铁。
[0371]
通过如上述那样实施铁分离方法m150,能够分离得到钨铁矿中所含的钨和铁。
[0372]
在溶解工序s1504中,作为将经加热工序s1503而得的液状混合物溶解的液体,还可以使用酸溶液(例如盐酸溶液)。这种情况下,钨铁矿中所含的铁溶解到盐酸溶液中,而钨铁矿中所含的钨留在固相中。像这样,单是在溶解工序s1504中使用酸溶液,就能获得溶解有铁的酸溶液。
[0373]
(实施例群)
[0374]
以下说明本发明的实施例群。在上述第1实施例和第2实施例中,分别使用绿柱石和锂辉石作为了起始物料。在以下的实施例群中,作为起始物料,使用了氧化硅、镍淤积物、钨铁矿、独居石、磷辉石、磷钇矿、铝土矿、磁铁矿、铁矿石、金红石以及闪锌矿。此外,在使用锂辉石作为起始物料的实施例中,作为在溶解工序s14中用以将混合物溶解的液体,使用了水。各实施例的结果总结在表1中。另外,在表1中也包括第1实施例以及第2实施例的结果。
[0375]
〔表1〕
[0376][0377]
表1中,“空心圆”符号代表的意思是:起始物料所含元素当中的作为对象溶质的元素至少得以了部分溶解。“叉”符号代表的意思是:作为对象溶质的元素未得到溶解。
[0378]
《第3实施例》
[0379]
在第3实施例中,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例中,使用了氧化硅(sio2)的高纯度试剂作为起始物料。另外,在本实施例中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。
[0380]
本实施例中,在粉碎
·
混合工序s12中混合的氧化硅与氢氧化钠的重量比设定为
1:10。此外,在加热工序s13中,用介电加热装置10在大气气氛、常压下进行介电加热。加热工序s13中的加热温度设定为300℃,加热时间设定为8分钟。通过实施加热工序s13,粉末状混合物随着介电加热而熔解,8分钟后全部成为乳液状的液状混合物。下文中,如果不需要区分混合物是粉末状还是液状,则简称为混合物。此外,在本实施例中,既采用盐酸溶液作为在溶解工序s14中用以将混合物溶解的液体来进行了实施,又采用水作为在溶解工序s14中用以将混合物溶解的液体来进行了实施。
[0381]
当将盐酸溶液用作将混合物溶解的液体时,产生了硅酸(h2sio4)的沉淀。可以认为,硅酸是作为起始物料的氧化硅经两个反应后所生成的。第1个反应是氧化硅与氢氧化钠反应而生成钠硅酸盐(na2sio4)的反应。钠硅酸盐具有水溶性,因此溶于溶液中。第2个反应中,钠硅酸盐与盐酸反应,从而生成硅酸。由于硅酸具有不溶性,因此溶液中产生了硅酸的沉淀。需要说明的是,使用水来替代盐酸时,并未产生沉淀,从这一点也可以确知使用了盐酸溶液来作为将混合物溶解的液体时,发生了上述2种反应。因此在表1中,用空心的
“△”
符号来代表将氧化硅用作起始物料且使用盐酸溶液来作为将用以混合物溶解的液体时的结果。
[0382]
需要说明的是,使用水来作为将混合物溶解的液体时,可以认为硅是以具有水溶性的钠硅酸盐方式溶解在溶液中的。这种情况下,氧化硅得以溶解的溶解度为90%以上。
[0383]
如上所述,本实施例中将氧化硅用作了起始物料。玻璃材料(例如石英玻璃)和硅石的主要成分也是氧化硅。因此,采用玻璃材料(例如石英玻璃)和硅石时,同样也可得到第3实施例的结果。
[0384]
《第4实施例群》
[0385]
在第4实施例群中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将氧化铝(al2o3)试剂用作起始物料。本实施例群中,采用模拟铝土矿的氧化铝来作为起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。此外,在本实施例群中,既采用盐酸溶液作为在溶解工序s14中用以将混合物溶解的液体来进行了实施,又采用水作为在溶解工序s14中用以将混合物溶解的液体来进行了实施。
[0386]
无论使用盐酸溶液还是使用水来作为用以将混合物溶解的液体,实施溶解工序s14后都得到了白浊的溶液。这些白浊溶液的分析结果表明,氧化铝会溶解于盐酸水溶液及水这两者中。铝相对于盐酸水溶液的溶解度为99%,铝相对于水的溶解度为95%。
[0387]
《第5实施例群》
[0388]
在第5实施例群中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将氧化钛(tio2)试剂用作起始物料。此外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物与在溶解工序s14中用以将混合物溶解的液体的组合,采用了如下组合:(1)氢氧化钠与盐酸溶液;(2)氢氧化钠与硫酸溶液;(3)氢氧化钾与硫酸溶液。
[0389]
无论上述(1)、(2)和(3)的哪种组合,在实施例了溶解工序s14后都得到了含有残渣的白浊溶液。得到的残渣的分析结果表明,氧化钛会溶解于酸溶液中。分别采用(1)、(2)及(3)所示组合而得的结果是,钛得以溶解的溶解度分别为25%、50%及98%。表1的有关氧化钛的栏目中,记载了采用(3)所示组合时的结果。
[0390]
《第6实施例群》
[0391]
在第6实施例群中,实施了图1所示的制造方法m10中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将氧化铍(beo)试剂用作起始物料。在本实施例群中,采用了氧化铍作为起始物料,以模仿中子倍增材料的一例即铍的表面上所形成的氧化铍。其理由在于:已知铍易溶于酸溶液;已作为中子倍增材料用过了的废旧铍的表面上形成有氧化铍。
[0392]
另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。此外,在本实施例群中,既采用盐酸溶液作为在溶解工序s14中用以将混合物溶解的液体来进行了实施,又采用水作为在溶解工序s14中用以将混合物溶解的液体来进行了实施。
[0393]
无论使用盐酸溶液还是使用水来作为用以将混合物溶解的液体,实施溶解工序s14后都得到了含有残渣的白浊溶液。得到的残渣的分析结果表明,氧化铍会溶解于盐酸水溶液及水这两者中。铍相对于盐酸水溶液的溶解度为90%,铍相对于水的溶解度为77%。
[0394]
《第7实施例群》
[0395]
在第7实施例群中,实施了图1所示的制造方法m10中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将钛酸锂(li2tio3)试剂用作起始物料。钛酸锂是氚增殖材料的一个例子。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。此外,在本实施例群中,既采用硫酸溶液作为在溶解工序s14中用以将混合物溶解的液体来进行了实施,又采用水作为在溶解工序s14中用以将混合物溶解的液体来进行了实施。
[0396]
无论使用硫酸溶液还是使用水来作为用以将混合物溶解的液体,实施溶解工序s14后都得到了含有残渣的白浊溶液。得到的残渣的分析结果表明,钛酸锂会溶解于硫酸水溶液及水这两者中。锂相对于硫酸水溶液的溶解度为97%,锂相对于水的溶解度为19%。
[0397]
《第1、第2、第8实施例》
[0398]
如第1实施例中所说明的那样,绿柱石完全溶解在了盐酸水溶液中(确认到有99%的铍得以溶解)。另外,如在第2实施例中说明的那样,锂辉石溶解在了盐酸水溶液中(确认到有90%以上的锂得以溶解)。另外,作为第1实施例的变形例,将在溶解工序s14中用以将液状混合物溶解的液体从盐酸水溶液变更为水。该变形例中,绿柱石中含有的铍得以溶解的溶解度为56%。
[0399]
另外,作为第8实施例,与第2实施例同样地将锂辉石用作起始物料,作为用以将混合物溶解的液体,使用了水。其结果,锂辉石溶于水(确认到有96%的锂得以溶解)中。
[0400]
《第9实施例》
[0401]
在第9实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例中,使用独居石((ce,la,nd,th)po4)作为起始物料。另外,在本实施例中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。另外,在本实施例中,加热工序s13中的加热温度为250℃。此外,在本实施例中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸溶液。
[0402]
实施溶解工序s14后,得到了黄色混浊的溶液。该溶液的分析结果如图19所示。图19是示出独居石所含的钇(y)、镧(la)、铈(ce)、钕(nd)、钐(sm)、铽(tb)和镝(dy)的溶解度的柱图。如图19所示,钇的溶解度约为80%,镧、钕、钐、铽和镝的溶解度分别为50%以上且
65%以下,铈的溶解度约为20%。
[0403]
《第10实施例》
[0404]
在第10实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例中,将磷辉石(ce5(po4)3(f,cl,oh)1)用作起始物料。另外,在本实施例中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。另外,在本实施例中,加热工序s13中的加热温度为250℃。此外,在本实施例中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸溶液。
[0405]
实施溶解工序s14后,得到了几乎没有残渣的溶液。分析该溶液后得知,磷辉石得以溶解的溶解度为90%以上。
[0406]
《第11实施例》
[0407]
在第11实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例中,使用磷钇矿(ypo4)作为起始物料。另外,在本实施例中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。另外,在本实施例中,加热工序s13中的加热温度为250℃。此外,在本实施例中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸溶液。
[0408]
实施溶解工序s14后得知,磷钇矿得以溶解的溶解度约为50%。
[0409]
《第12、13实施例》
[0410]
在第12实施例和第13实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在第12实施例中使用磁铁矿(fe3o4)作为起始物料,在第13实施例中使用铁矿石(fe2o3)作为起始物料。另外,在本实施例中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。另外,在本实施例中,加热工序s13中的加热温度为250℃。此外,在本实施例中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸溶液。
[0411]
对实施溶解工序s14后所得的残渣进行分析后得知,磁铁矿得以溶解的溶解度在90%以上,铁矿石得以溶解的溶解度也在90%以上。另外,还使用磁铁矿作为起始物料且使用水作为用以将混合物溶解的液体来进行了实施。但这种情况下,磁铁矿和铁矿石未能得以溶解。
[0412]
《第14实施例》
[0413]
在第14实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例中,将辉钼矿(mos2)用作起始物料。另外,在本实施例中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。另外,在本实施例中,加热工序s13中的加热温度为250℃。此外,在本实施例中,作为在溶解工序s14中用以将混合物溶解的液体,使用了(1)盐酸溶液、(2)2m硝酸溶液、(3)硫酸与硝酸的混合溶液、以及(4)5m硝酸溶液。
[0414]
对溶解工序s14后得到的残渣进行了分析后得知,分别就(1)~(4)所示的溶液看,钼得以的溶解度分别为25%、44%、62%和65%。表1的有关辉钼矿的栏中,记载了采用(3)和(4)所示溶液时的结果。
[0415]
《第15实施例群》
[0416]
在第15实施例群中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉
碎
·
混合工序s12~溶解工序s14。在本实施例中,将闪锌矿((zn,fe)s)用作起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。此外,在本实施例群中,既采用盐酸溶液作为在溶解工序s14中用以将混合物溶解的液体来进行了实施,又采用水作为在溶解工序s14中用以将混合物溶解的液体来进行了实施。
[0417]
无论使用盐酸溶液还是使用水来作为用以将混合物溶解的液体,实施溶解工序s14后都得到了含有残渣的混浊溶液。得到的残渣的分析结果表明,闪锌矿会溶解于盐酸水溶液及水这两者中。闪锌矿相对于盐酸水溶液的溶解度为90%以上,铝相对于水的溶解度为80%以上。
[0418]
《第16实施例及第17实施例》
[0419]
在第16实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将钨铁矿(fewo4)用作起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。此外,在本实施例群中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸溶液。
[0420]
在第17实施例中,实施了图18所示的分离方法m150。本实施例群中,将钨铁矿(fewo4)用作起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠。此外,在本实施例群中,作为在溶解工序s14中用以将混合物溶解的液体,使用了水。
[0421]
第16实施例中,在实施了溶解工序s14后,得到了含有残渣的混浊溶液。得到的残渣的分析结果表明,钨铁矿中所含的铁得以溶解的溶解度在90%以上。但在该混浊的溶液中,含钨的化合物作为残渣沉淀。
[0422]
关于第17实施例,在实施了溶解工序s1504后,得到了含有残渣的混浊溶液。得到的残渣的分析结果表明,钨铁矿中所含钨的溶解度在90%以上。但在该混浊的溶液中,含铁的化合物作为残渣沉淀。继而实施了盐酸浸渍工序s1552及第3过滤工序s1553,得到了透明的溶液。该溶液的分析结果表明,钨铁矿中所含的铁得以溶解的溶解度在90%以上。
[0423]
《第18实施例》
[0424]
在第18实施例中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将富钴结壳用作起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钾。此外,在本实施例群中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸溶液。
[0425]
第18实施例中,在实施了溶解工序s14后,得到了含有少量残渣的溶液。该残渣的分析结果表明,富钴结壳得以溶解的溶解度约为95%。
[0426]
《第19实施例群》
[0427]
在第19实施例群中,与第3实施例同样地,实施了图12所示的制造方法m90中的粉碎
·
混合工序s12~溶解工序s14。在本实施例群中,将锰结核用作起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠和氢氧化钾。另外,在本实施例群中,加热工序s13中的加热温度为250℃。此外,在本实施例群中,作为在溶解工序s14中用以将混合物溶解的液体,使用了盐酸及水。作为氢氧化物与上述液体的组合,采用了如下组合:(1)氢氧化钠与盐酸溶液;(2)氢氧化钠与水;(3)氢氧化钾与盐酸溶液。表1的有关锰结核的栏目中记载了采用(2)和(3)所示组合时的情况。
[0428]
无论上述(1)、(2)和(3)的哪种组合,在实施了溶解工序s14后都得到了含有残渣的溶液。对分别采用(1)、(2)和(3)所示组合而得到的残渣进行分析后发现,锰结核得以溶解的溶解度约为56%、27%和85%。
[0429]
《第20实施例群》
[0430]
在第20实施例群中,实施了图17所示的制造方法m140。在本实施例群中,将镍淤积物用作起始物料。另外,在本实施例群中,作为在粉碎
·
混合工序s12中混合的氢氧化物,使用了氢氧化钠和氢氧化钾。此外,在本实施例群中,作为在溶解工序s14中用以将混合物溶解的液体,使用了水。需要说明的是,在第20实施例群中,在实施了制造方法m140后,对获得的固相再次实施了制造方法m140。
[0431]
在使用氢氧化钠作为氢氧化物的情况下,实施了第1次溶解工序s1404后得到了含有残渣的淡黄色溶液。分析该淡黄色溶液后得知,氟离子的浓度为16.7%,硫离子的浓度为3.4%。另外,未检测到镍。另外,对实施了第2次溶解工序s1404后得到的溶液进行分析后得知,氟离子的浓度为0.5%,硫离子的浓度为0.3%。
[0432]
在使用氢氧化钾作为氢氧化物的情况下,实施了第1次溶解工序s1404后得到了含有残渣的淡黄色溶液。分析该淡黄色溶液后得知,氟离子的浓度为15.8%,硫离子的浓度为3.3%。另外,未检测到镍。另外,对实施了第2次溶解工序s1404后得到的溶液进行分析后得知,氟离子的浓度为0.5%,硫离子的浓度低于检测极限。
[0433]
根据以上结果可知,通过实施制造方法m140,能使作为起始物料的镍淤积物中所含的氟离子和硫离子溶解到溶液中,从而能将镍淤积物中所含镍的纯度提高。
[0434]
(总结)
[0435]
本发明第1方面的无机物溶液的制造方法包括:加热工序,对将无机物的粉末与氢氧化物混合而成的粉末状混合物进行介电加热,从而得到含有上述无机物的液状混合物。予以说明,本制造方法中,氢氧化物的形状不受限制。
[0436]
氢氧化物所含的氢氧基通过吸收用于介电加热的电磁波,来将该电磁波的能量转化为自身的热能。在本制造方法的加热过程中,由于无机物的粉末与氢氧化物的粉末为彼此混合状态,因此氢氧化物的热能也有效地提供于无机物。其结果,可以获得由无机物和氢氧化物熔解而成的液状混合物。该液状混合物易溶解于酸溶液。因此,能通过采用该液状混合物来制造无机物溶液。
[0437]
此外,在加热过程中,不需要像非专利文献1中记载的烧结处理或熔融处理那样在高温(例如770℃、1650℃、2000℃等)下进行处理,只需对粉末状混合物实施介电加热即可获得液状混合物。因此,与非专利文献1中记载的制造方法相比,本制造方法的能效高。
[0438]
如上所述,本发明提供的制造方法为一种高能效的新型制造方法,其用以制造诸如铍矿这类既难溶于碱性溶液又难溶于酸性溶液的无机物的溶液。
[0439]
另外,在本发明第2方面的无机物溶液的制造方法中,在上述第1方面的制造方法的方案的基础上,还采用以下的方案:上述无机物包含铍及锂中的至少一者。
[0440]
如此,作为无机物的一例,可举出含有铍及锂中至少一者的物质。
[0441]
另外,在本发明第3方面的无机物溶液的制造方法中,在上述第1方面或第2方面的无机物溶液的制造方法的方案的基础上,还采用以下的方案:上述氢氧化物是氢氧化钠和氢氧化钾中的至少一者。
[0442]
如此,作为氢氧化物的一例,可举出氢氧化钠及氢氧化钾。另外,作为氢氧化物,也可以采用由氢氧化钠与氢氧化钾组成的混合物。
[0443]
另外,在本发明第4方面的无机物溶液的制造方法中,在上述第1方面~第3方面中的任一方面的无机物溶液的制造方法的方案的基础上,还采用以下的方案:还包括溶解工序,所述溶解工序使经上述加热工序而得的上述液状混合物溶解于酸溶液或水中,从而得到上述无机物的酸溶液。
[0444]
根据上述方案,可以切实地获得无机物溶液。
[0445]
另外,在本发明第5方面的无机物溶液的制造方法中,在上述第1方面~第4方面中的任一方面的无机物溶液的制造方法的方案的基础上,还采用以下的方案:上述加热工序是在常压下对上述粉末状混合物进行介电加热的工序。
[0446]
如此,在本制造方法的加热工序中,即使在不加压的条件下对粉末混合物进行介电加热,也可以获得液状混合物。因此,能将用以实施本制造方法的制造装置构造设计得简单,还能节省为了在工厂中设置制造装置而需的申报劳力。
[0447]
本发明第6方面的无机物溶液的制造装置具备:混合部,其用以将无机物的粉末与氢氧化物混合来得到由无机物及氢氧化物组成的粉末状混合物;容器,其用以容纳上述粉末状混合物;电磁波产生部,其产生用于进行介电加热的电磁波。
[0448]
根据上述方案,起到与上述第1方面的无机物溶液的制造方法同样的效果。予以说明,在本制造装置的混合部中与无机物的粉末进行混合的氢氧化物的形状不受限制。
[0449]
另外,在本发明第7方面的无机物溶液的制造装置中,在上述的第6方面的无机物溶液的制造装置的方案的基础上,还采用以下的方案:上述无机物包含铍及锂中的至少一者。
[0450]
根据上述方案,起到与上述第2方面的无机物溶液的制造方法同样的效果。
[0451]
另外,在本发明第8方面的无机物溶液的制造装置中,在上述第6方面或第7方面的无机物溶液的制造装置的方案的基础上,还采用以下的方案:上述氢氧化物是氢氧化钠和氢氧化钾中的至少一者。
[0452]
根据上述方案,起到与上述第3方面的无机物溶液的制造方法同样的效果。另外,作为氢氧化物,也可以采用由氢氧化钠与氢氧化钾组成的混合物。
[0453]
另外,在本发明第9方面的无机物溶液的制造装置中,在上述第6方面~第8方面中的任一方面的无机物溶液的制造装置的方案的基础上,还采用以下的方案:还具备波导管及隔离器,波导管介于上述电磁波产生部与上述容器之间,并且将上述电磁波从上述电磁波产生部传导至上述容器,隔离器设置在上述波导管的中途区段,并且吸收从上述容器向电磁波产生部传播的电磁波。
[0454]
根据上述方案,即使电磁波产生部产生的电磁波的一部分沿着从容器前往电磁波产生部的方向返回,隔离器也能够吸收该电磁波。因此,可以抑制对电磁波产生部的工作产生的不良影响。
[0455]
另外,在本发明第10方面的无机物溶液的制造装置中,在上述第6方面~第9方面中的任一方面的无机物溶液的制造装置的方案的基础上,还采用以下的方案:还具备用以向上述容器供给酸溶液或水的液体供给部。
[0456]
根据上述方案,起到与上述第4方面的无机物溶液的制造方法同样的效果。
[0457]
(附注)
[0458]
本发明不限于上述各实施方式,在说明书所示的范围内可以进行各种变更,并且通过适当地组合在不同实施方式中公开的技术手段而获得的实施方式也包括在本发明的技术范围内。
当前第1页1
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!